2-2. ОСНОВНЫЕ СВЕДЕНИЯ О РАСТВОРИТЕЛЯХ
Растворителями называются органические летучие жидкости, которые способны растворять такие вещества, как жиры, натуральные и синтетические смолы, воски, асфальты, каучуки и др. Растворы этих веществ можно получать различных концентраций в зависимости от растворяющей способности растворителя и растворимости того или иного вещества.
Жидкости, которые применяются для снижения вязкости (разбавления) готовых растворов, называются разбавителями. Нелетучие специальные жидкости, которые остаются в пленке после ее высыхания и предназначены для увеличения гибкости пленки, называются пластификаторами.
Из многих теорий, трактующих процесс растворения, большое распространение имеет теория Лэнгмюра—Гильдебранта, согласно которой растворение вещества зависит от наличия в растворяемом веществе и растворителе полярных или неполярных групп. При взаимодействии диполей полярных веществ (молекулярная когезия) происходит молекулярная ассоциация. Если встречаются полярные и неполярные молекулы, образование молекулярной ассоциации затрудняется. В этом случае возможно отталкивание молекул одной группы от молекул других групп и растворение пли смешение веществ не происходит. Таким же образом можно представить и процесс растворения твердых веществ, который будет активно проходить в полярных растворителях, если растворяемое вещество будет полярным, и наоборот.
Различают истинные (кристаллоидные) и коллоидные растворы. Строгое разграничение обоих типов растворов затруднительно, так как растворяемые вещества с очень большой молекулярной массой образуют растворы, которые находятся в граничной области между кристаллоидными и коллоидными растворами.
Β истинных растворах растворитель проникает глубоко в растворяемое вещество и разделяет его на отдельные молекулы. Такие растворы представляют собой гомогенную смесь, в которой молекулы растворителя и растворимого вещества находятся в свободном состоянии. Если растворитель соприкасается с коллоидообразующим веществом, то в последнем наступает разрыхление структуры, которое прежде всего проявляется в набухании внешних слоев. Большие молекулы коллоидов или их агрегаты связывают много молекул растворителя, и поэтому полное разделение молекул растворяемого вещества и растворителя невозможно. Коллоидные растворы отличаются от истинных еще и тем, что для них не существует определенного для той или иной температуры предела растворимости и поэтому растворяющая способность растворителей в этом случае определяется несколько другими методами, чем у истинных растворов.
Растворители оказывают значительное влияние на качество готовой пленки. Например, быстро испаряющийся растворитель может нарушить целостность образующейся пленки; наличие в растворителе трудно испаряющихся частей оказывает пластифицирующее действие на пленку. Активность растворителя определяется скоростью растворения пленкообразователя, осаждением его из раствора при понижении температуры (чем ниже температура осаждения, тем активнее растворитель), сравнением вязкости растворов при одинаковой концентрации пленкообразователя (чем меньше вязкость, тем активнее растворитель) и осаждением пленкообразователя из раствора при добавлении разбавителя. Отношение объема разбавителя к объему растворителя может служить мерой растворяющей способности растворителя. Для ароматических углеводородов это отношение больше, чем для алифатических.
Жидкости с малой молекулярной массой обладают большей растворяющей способностью, чем жидкости с большой молекулярной массой.
Растворители обладают высокой упругостью пара. Последняя обычно характеризуется температурой кипения растворителя, т. е. той температурой, при которой упругость паров становится равной атмосферному давлению.
По температуре кипения растворители можно классифицировать следующим образом: 1) низкокипящие растворители с температурой кипения 30—70°C; 2) среднекипящие растворители с температурой кипения 70— 110 °C; 3) высококипящие растворители с температурой кипения 110—170 °C.
Растворители, температура кипения которых находится в пределах 200—300 °C, неудобны для применения вследствие весьма медленного их улетучивания. Жидкости, температура кипения которых выше 300 °C, обычно относятся к пластификаторам. На практике летучесть растворителей часто характеризуется временем испарения капли растворителя, нанесенной на фильтровальную бумагу, причем за единицу летучести принимается время испарения серного эфира (табл. 2-1).
Большинство летучих растворителей являются весьма горючими веществами, пары которых в смеси с воздухом могут образовывать вспыхивающие и даже гремучие смеси. Огнеопасность растворителей, которые могут вызвать взрыв, помимо объемной концентрации паров (%), в известной степени характеризует также температура кипения, вспышки (воспламенения) паров и самовоспламенения жидкости (табл. 2-1).
Таблица 2-1
Физические свойства растворителей
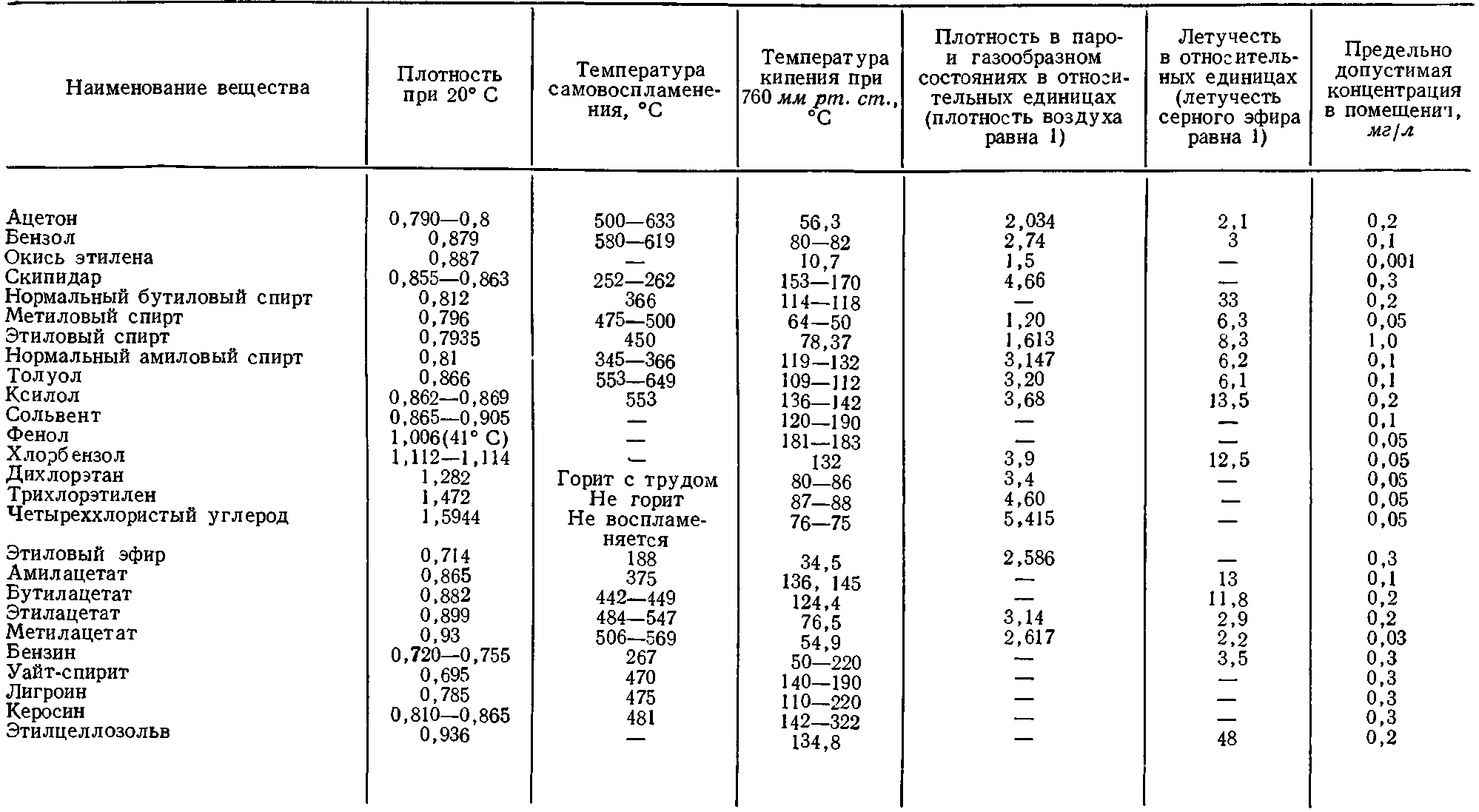
Все летучие растворители в той или иной степени токсичны. Более опасными в этом отношении являются легколетучие растворители, так как обычно они содержатся в воздухе в большем количестве, чем высококипящие растворители. Наиболее вредными являются галоидопроизводные вещества (четыреххлористый углерод, дихлорэтан, хлорбензол и т. п.), действующие как наркотики. Вредными являются также ароматические углеводороды (бензол, толуол и отчасти ксилол, сольвент), а также метиловый спирт, длительное вдыхание паров которого оказывает вредное действие на зрение и мозговую деятельность. Применяемые иногда в качестве растворителей фенол и крезол также относятся к вредным веществам, так как, помимо высокой токсичности паров, при непосредственном воздействии фенол и крезол вызывают ожоги и заболевание кожи.
Растворители повышенной токсичности находят весьма ограниченное применение в производстве эмалированных проводов. В отдельных случаях, когда они все же применяются, принимаются особые меры (герметизация лаковых ванн, усиленная вентиляция эмалировочных цехов и т. п., которые исключают вредное действие этих растворителей.
Применяемый в производстве эмалированных проводов в качестве растворителя масляно-смоляных лаков осветительный керосин является одним из наименее токсичных растворителей. То же самое можно сказать и про бензины различных марок, причем содержание ароматических углеводородов в составе последних составляет всего 6—8%, а у керосина из различных нефтей оно колеблется в пределах 11—18%.
В табл. 2-1 и далее в тексте приведены основные сведения о растворителях, имеющих наибольшее применение в производстве эмалированных проводов.
Керосин. В качестве растворителя масляных эмаль-лаков в типовой технологии кабельных заводов Советского Союза принят осветительный керосин. Для изготовления этого керосина применяются дистилляты прямой перегонки нефти с температурой кипения в пределах 180—315°C. Для удаления смол и нафтеновых кислот керосиновые дистилляты подвергаются сернокислотной очистке. Существует несколько разновидностей осветительного керосина, на которые распространяются специальные ТУ и стандарты. При изготовлении эмаль-лаков применяется осветительный керосин, на который распространяются технические условия НП БТУ 4-58. Этот керосин изготовляется из эмбенских бессернистых нефтей и имеет окраску от бесцветной до светло-желтой.
Температура начала кипения этого керосина не ниже 170°C; 50% объема керосина должно выкипать при температуре не выше 250 °C, 90% — при температуре не выше 270 °C и 98% — при температуре не выше 315°C. Кислотное число этого керосина не выше 1,4, зольность не более 0,005, содержание серы не более 0,05%. Температура вспышки паров в смеси с воздухом не ниже 50 °C.
Скипидар.
В производстве эмаль-лаков иногда применяется живичный скипидар (терпентинное масло) для добавления в отдельных случаях в количестве 5% общего количества керосина при разведении лака МЛ-3 для эмалирования проволоки диаметром 0,05—0,09 мм. На этот скипидар распространяется ГОСТ 1'571-66. Скипидар представляет собой жидкость с характерным приятным запахом. В соответствии с указанным ГОСТ скипидар выпускается двух марок: А и Б. Плотность скипидара обеих марок при 20 °C должна быть в пределах 0,855—0,863, а температура начала кипения — в пределах 153—160 °C. Объем отгона до температуры 170 °C у скипидара марки А должен быть не менее 92% и у марки Б не менее 80%. Остаток после испарения должен быть не более 0,5% (марка А) и 1% (марка Б), а кислотное число — соответственно не более 0,7 и 1,8. В кабельной промышленности обычно применяется скипидар марки А, который по внешнему виду значительно светлее скипидара марки Б.
Этилцеллозольв.
Этилцеллозольв представляет собой моноэтиловый эфир этиленгликоля и получается при взаимодействии окиси этилена (ГОСТ 7568-55) и этилового спирта (ГОСТ 5262-51) с последующей ректификацией. Его химическая формула СН2ОН— СН2(ОС2Н5). По внешнему виду этилцеллозольв представляет собой прозрачную бесцветную жидкость, имеющую плотность в пределах 0,930—0,935; в зависимости от назначения он выпускается двух марок (А и Б). Содержание этилцеллозольва в жидкости марки А должно быть не менее 94%, а марки Б не менее 92%. Фракция, выкипающая при температуре 128—138°С, у этилцеллозольва марки А должна составлять не менее 94%, а марки Б — не менее 92%. Кислотное число у этилцеллозольва обеих марок должно быть не более 2,5 мг КОН на 1 г продукта, сухой остаток — не более 0,005%; смешиваемость с водой — хорошая.
Бензол С6Н6 — углеводород ароматического ряда — является одним из наиболее распространенных растворителей. Он хорошо растворяет масла, простые и сложные эфиры целлюлозы, многие смолы, каучук, асфальты и пр. По внешнему виду бензол представляет собой бесцветную прозрачную и летучую жидкость плотностью 0,876—0,880 с температурой плавления не ниже 5,0— 5,4 °C и начала кипения 79,0—79,6 °C. Бензол хорошо растворяется в этиловом спирте, ацетоне, эфире и т. п.; в воде бензол нерастворим. Помимо высокой токсичности (пары бензола ядовиты и оказывают наркотическое действие), бензол весьма горюч. Он имеет низкую температуру воспламенения (около +8°C); при содержании паров бензола в воздухе в количестве 1,5—8,0% образуется взрывчатая смесь. Поэтому при обращении с бензолом и его хранении необходимо принятие строгих противопожарных мер. В настоящее время па бензол каменноугольный распространяется ГОСТ 8448-61, в соответствии с которым бензол изготовляется нескольких марок: «особо чистый», «чистый для синтеза» (4-го и 2-го сортов), «чистый для нитрации» (1-го и 2-го сортов), «чистый» и 90%-ный.
Температура окончания процесса перегонки бензола всех марок (кроме 90%-ного) не выше 80,3—80,6 °C. Таким образом, бензол перегоняется в очень узком температурном интервале. В соответствии с ГОСТ 8448-61 95% всего объема должны перегоняться при разности температур не более 0,6—1,0 °C.
Толуол С6Н5ОН3 также относится к растворителям ароматического ряда. Как растворитель он действует аналогично бензолу, за исключением сложных эфиров, которые толуол не растворяет, но может применяться как разбавитель их растворов. Толуол — весьма горючая прозрачная бесцветная жидкость с плотностью 0,856— 0,866 менее ядовитая, чем бензол. Он испаряется без остатка в температурном интервале 109—111 °C.
Ксилол СН3С6Н4СН3 — также углеводород ароматического ряда — является хорошим растворителем масел и смоляных эфиров; он смешивается с углеводородами нефти и растворителями эфиров целлюлозы. Температура вспышки паров около 29 ° С. Ксилол представляет собой прозрачную и бесцветную жидкость. В соответствии с ГОСТ 9949-62 он выпускается марок А и Б. Температура начала перегонки ксилола 136,5—137 °C, а конца этого процесса 141—141,5 °C, причем 95% ксилола марки А перегоняются в интервале температур не более 3°С, а марки Б — не более 4,5 °C. Кроме того, ксилол марки А имеет несколько более высокую степень очистки по сравнению с ксилолом марки Б.
Сольвент каменноугольный — смесь ароматических углеводородов — от других растворителей этого типа отличается несколько меньшими токсичностью и горючестью, является хорошим растворителем масляных, глифталевых и асфальтовых лаков. Однако и сольвент каменноугольный из-за свойственного ему запаха и токсичности ограничен в применении в качестве растворителя в производстве эмалированных проводов. Он получается в коксохимическом производстве в процессе ректификации очищенных фракций сырого бензола и в соответствии с ГОСТ 1928-67 изготовляется трех марок: А, Б и В. Сольвент каменноугольный марок А и Б — бесцветная прозрачная жидкость плотностью соответственно 0,865—0,875. Температура начала процесса перегонки 126°C, окончания отгонки 90% 160—170°C. Сольвент марки В представляет собой прозрачную жидкость светло-желтого цвета плотностью 0,885±0,02 с температурой начала перегонки 135°C и окончания отгонки 90% не выше 190 °C. Сольвент каменноугольный имеет нейтральную реакцию водной вытяжки, содержание фенола не более 0,01—0,1%, серы не более 0,10—0,30%.
Хлорбензол С6Н5С1 получается хлорированием бензола, причем обычно он содержит в качестве примеси некоторое количество дихлорбензола. Хлорбензол является активным растворителем и к тому же хорошо смешивается с другими растворителями. По внешнему виду хлорбензол представляет собой бесцветную жидкость со слабым миндальным запахом и в соответствии с ГОСТ 646-60 изготовляется двух марок А (1-го и 2-го сортов) и Б. Хлорбензол марки А предназначается для синтеза чистых и технических органических продуктов, а марки Б — для синтеза продуктов с пониженными требованиями к исходному сырью и для прочих технических целей. Хлорбензол является весьма хорошим растворителем для многих лаков; он содержит бензола в зависимости от марки не более 0,1—0,3%, полихлоридов — не более 0,75—1,0%, реакция водной вытяжки нейтральная. Одной из основных характеристик хлорбензола в соответствии с ГОСТ 646-60 является его способность перегоняться в количестве 95% в пределах изменений температуры для марки А (1-й сорт) не более 0,7 °C, для марки А (2-й сорт) не более 2 °C и для марки Б не более 3,5 °C.
Недостатком хлорбензола, кроме его токсичности, является невозможность каталитического сжигания отходящих паров этого растворителя в эмаль-печах, что затрудняет его применение при изготовлении эмалированных проводов на новейшем технологическом оборудовании.
Ацетон СH3COCH3 по своему химическому составу относится к кетонам. Чистый ацетон — лепкоподвижная бесцветная жидкость плотностью 0,790—0,799; температура вспышки паров около 17°С. Ацетон смешивается с водой в любых соотношениях, растворяется в спирте, метиловом и этиловом эфирах, хлороформе и т. п., хорошо растворяет многие смолы и масла, а также нитро- и ацетилцеллюлозу. Ввиду высокой летучести очень огнеопасен. В соответствии с ГОСТ 2768-67 он выпускается двух марок: А и Б с содержанием ацетона соответственно не менее 99,5 и 98,5%, а воды не более 0,5 и 1,5%. У ацетона марки А при 55,5—56,5 °C должно отгоняться не менее 97% объема, а у ацетона марки Б при 55,5— 57,0°C — не менее 95%. Содержание нелетучего остатка у ацетона марки А не более 0,002%, у марки Б — не более 0,003%.
Фенолами называются производные ароматических углеводородов, в молекулах которых один или несколько водородных атомов бензольного ядра замещены гидроксильными группами. Фенол С6Н5ОН и некоторые его гомологи (крезол и др.) получаются при фракционной перегонке каменноугольного дегтя. Фенол, называемый обычно карболовой кислотой, представляет собой бесцветную или светло-желтую кристаллическую массу, состоящую из длинных игл. Он затвердевает при 39,7— 40,3 °C и кипит при 181—1183 °C. Фенол при определенных условиях растворяется в воде. Кроме того, добавление в фенол нескольких процентов воды понижает температуру плавления смеси настолько, что она при комнатной температуре превращается в жидкость.
Таблица 2-2
Примерное содержание изомеров в трикрезоле и их свойства

Фенол и крезол (СН3С6Н4ОН) находят применение в качестве антисептиков и дезинфицирующих веществ. В производстве эмалированных проводов эти углеводороды иногда применяются в качестве растворителей синтетических лаков на полиамидной и поливинилацеталевой основах. Креозол существует в виде трех изомеров:
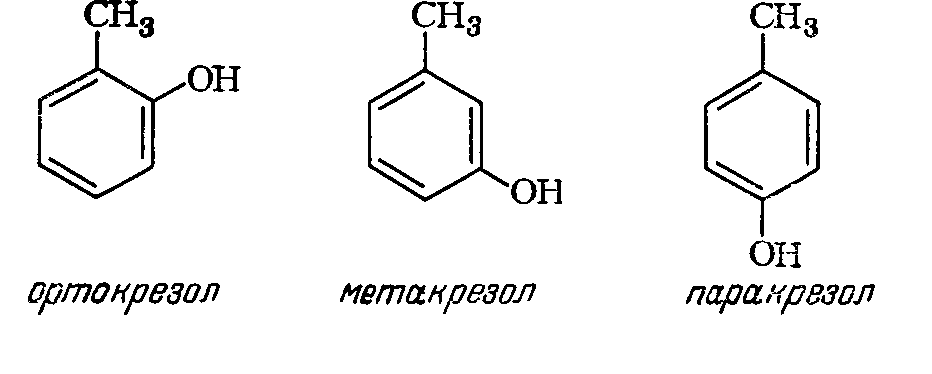
Технический крезол (трикрезол) представляет собой смесь всех трех изомеров. Его плотность 1,03—1,05, температура кипения в пределах 185—205 °C. Трикрезол растворим в спирте, эфире и растворах едких щелочей; 2,5 части трикрезола растворяются в 100 частях воды. Разделение изомеров крезола затруднительно ввиду близости температур кипения изомеров. Ортокрезол можно получить тщательной разгонкой, так как его температура кипения ниже температуры кипения других изомеров. Разделение мета- и паракрезола представляет большие трудности, и эти изомеры обычно сопутствуют один другому. Примерное содержание изомеров в трикрезоле и их характеристики приведены в табл. 2-2.

