Радионуклиды обладают различной биологической эффективностью. По своему биологическому действию радиоактивные вещества различаются между собой в зависимости от вида, энергии излучения, периода полураспада, величины всасывания, накопления и скорости выведения из организма.
Наибольший биологический эффект при попадании внутрь организма отмечается от воздействия α-излучателей, в связи с высокой их плотностью ионизации в тканях. Некоторые исследователи считают, что биологическая эффективность α-активных веществ в 10 раз больше, чем эффективность β-излучателей. Несколько меньшую опасность для организма представляют β- и γ-излучатели.
Таблица 1.5. Значение коэффициента качества

Эффективность α-частиц при попадании в организм зависит от микрораспределения их в органах и тканях. Однако, когда энергия α-частиц поглощается в малочувствительных элементах органа (например, в структурах, содержащих известь), α-излучатель может быть менее эффективен, чем β-излучатель. Так, остеотропный α-излучатель 226Ra менее эффективен, чем β-излучатели 90Sr, 90Y, 140Ba [74].
Биологический эффект от β-излучателей определяется энергией электронов. При остром лучевом воздействии мягкие β-излучатели 3Н, 95Nb, 147Ρm значительно эффективнее жестких 106Ru, 144Ce. Меньший биологический эффект в острой стадии поражения жесткими β-излучателями объясняется особенностями в микрогеометрии распределения их в органах и тканях, а также большей биологической эффективностью замедленных концов пробега β-частиц, число которых обычно пропорционально не ионизационной дозе, а числу распадов в беккерелях [130].
При определении эквивалентной дозы различных видов ионизирующих излучений используют коэффициент качества Q (табл. 1.5). При сравнении биологического действия различных излучателей необходимо учитывать их относительную биологическую эффективность (ОБЭ). Сравниваемые поглощенные дозы выражаются в зивертах (1 Зв=1 Γρ/Q). Зиверт (Зв) — единица эквивалентной дозы, учитывающая ОБЭ данного вида излучения. Радионуклиды с коротким не имеют выраженных различий между поглощенными дозами при остром, подостром и хроническом течении заболевания. В этом случае у животных наблюдается относительно быстрое восстановление гемопоэза и нарушений функций внутренних органов. Радионуклиды с длительным Тэф характеризуются значительными различиями в поглощенных дозах при острых и хронических воздействиях.
Таблица 1.6. Биологическое действие ионизирующего излучения

Биологическое действие ионизирующего излучения в организме условно разделяют на три уровня: физико-химический, клеточный и организменный или системный уровень [59, 67]. В табл. 1.6 показано развитие изменений в организме, возникающих при действии ионизирующего излучения.
Физико-химический уровень включает в себя все первичные процессы, протекающие в клетке. Ионизирующее излучение (рентгеновское, β- и γ-излучения, тяжелые ядерные частицы обладает высокой биологической активностью. Оно способно разрывать любые химические связи и индуцировать длительно протекающие реакции. При взаимодействии ионизирующего излучения с клетками и тканями в процессе превращения этого излучения в химическую энергию в организме зарождаются активные центры радиационно-химических реакций [59, 67].
В патогенезе лучевого поражения, вызванного ионизирующим излучением, определяющими являются первичные реакции, которые развиваются с большими ионными выходами и вовлекают в химические превращения сотни и тысячи молекул, чем значительно усиливают общий объем разрушений в клетках организма.
Первичное действие излучений на организм бывает непосредственным и косвенным. При непосредственном действии наблюдается расщепление атомов и молекул вещества, вызванное ионизацией. Вклад непрямого действия составляет не менее 50 % [23].
Основным актом взаимодействия ядерных излучений с тканями и клетками организма является ионизация, при которой происходит отрыв электронов от атомов, образование ионов и, кроме того, возникновение возбужденных атомов и появление радикалов. Эти активные молекулы и обломки молекул индуцируют различные реакции в тканях организма. В результате физико-химических процессов изменяется или повреждается структура макромолекулярных комплексов клеток.
Косвенное действие излучения проявляется в расщеплении молекул воды с образованием свободного водорода и пероксидов. Происходит изменение различных биохимических процессов в организме. Продукты расщепления вступают во взаимодействие с белковыми и липидными молекулами. В результате этого взаимодействия происходят структурные изменения тканей и клеток. Это ведет к гибели тканевых элементов, разрушению надмолекулярных структур (нитей хроматина), происходит разрыв углеродных связей, нарушение ферментных систем, синтеза ДНК, белка [133].
Подавление активности ферментов нарушает обменные процессы в организме, в связи с чем замедляется и прекращается роет тканей. Нарушение обмена веществ ведет к изменению химических процессов в клетках и их гибели. Всасывание продуктов клеточного распада вызывает отравление организма. Основные субстраты первичных окислительных реакций — нуклеопротеиды и биолипиды [59].
Клеточный уровень воздействия включает в себя все нарушения и процессы, обусловленные изменениями функциональных свойств облученных клеточных структур. Все процессы, протекающие на этом уровне, подчиняются биологическим законам жизни клетки как целостной, сложно функционирующей биологической системы. Наиболее опасными повреждениями клетки, возникающими при облучении, являются повреждения механизма митоза и хромосомного аппарата клеток облученной популяции. Количество клеток с такими повреждениями в облученной популяции находится в прямой зависимости от экспоненциальной дозы облучения, блокирования процессов дифференцировки, блокирования процессов физиологической регенерации и пролиферации облученных тканей. Указанные функциональные повреждения вызывают развитие большинства конечных эффектов воздействия ионизирующего излучения на организм многоклеточных и высших животных.
Изменения па клеточном уровне приводят к нарушению наследственных структур. Проявлениями этого поражения в результате облучения являются подавление органогенеза в эмбриональной стадии развития при облучении зародышей, угнетение гемопоэза во взрослом организме, подавление сперматогенеза и овогенеза, угнетение иммунореактивности.
Организменный, или системный, уровень включает в себя все процессы и изменения, связанные с нарушением функций организма. Биологическое действие ионизирующего излучения проявляется во всех органах и клетках живого организма. Наблюдаются изменения в кроветворной, периферической и центральной нервной системах. Это ведет к возникновению очагов повышенной возбудимости в коре и в периферических отделах нервной системы. Возникает дискорреляция между нервной системой и железами внутренней секреции, а также между другими системами организма.
Все процессы этих трех уровней взаимообусловлены и взаимосвязаны непосредственными и опосредованными прямыми и обратными связями. Наиболее радиочувствительными тканями организма являются дифференцирующие ткани. Радиочувствительность недиффереицирующихся тканей прямо зависит от скорости физиологических процессов инактивации — старения и отмирания клеточных элементов данной ткани [59].
Радиоактивные вещества при попадании в организм могут вызывать острое, подострое и хроническое лучевое поражение. Острое заболевание возникает от введения большой дозы радионуклидов. При этом отмечаются выраженные изменения в крови (лейкопения, ретикулопения), кровоизлияния в различные органы, угнетение иммунологической реактивности, снижение массы тела. Гибель животных наступает в течение первых двух недель.
Подострое поражение характеризуется изменениями лимфоидного и эритроидного ростков кроветворения. Наряду со снижением количества лейкоцитов снижается количество эритроцитов, гемоглобина и ретикулоцитов. Нарушается проницаемость сосудов, удлиняется время свертывания крови, уменьшается количество тромбоцитов, возникают инфекционные осложнения, падает масса тела. Животные гибнут через 1—3 мес после введения радионуклида.
Хроническое течение процесса связано с воздействием малых доз инкорпорированных радионуклидов. При этом в ранние сроки клинические явления могут отсутствовать. В крови отмечаются качественные изменения: анизоцитоз и пойкилоцитоз эритроцитов, токсическая зернистость нейтрофилов, вакуолизация протоплазмы, пикноз лимфоцитов. У животных наблюдаются снижение иммунологической реактивности, сосудистые расстройства, угнетение половой функции, раннее старение, сокращение продолжительности жизни, развиваются опухоли различных органов и тканей.
Биологическое действие малых доз радиоактивных веществ, не укорачивающих естественной продолжительности жизни, компенсируется защитными физиологическими функциями организма. Однако при изменении условий внешней среды и функционального состояния организма могут истощаться компенсаторные механизмы, и в отдаленные сроки после поражения может проявиться действие ионизирующего излучения. При этом специфику заболевания во многом определяет характер распределения радионуклида. Так, при воздействии остеотропных радионуклидов 90Sr, 140Bа, 226Ra, 239Pu выраженные изменения наблюдаются в костной ткани, кроветворной системе вследствие избирательного отложения их в костном мозге и, как следствие, его облучения. В отдаленные сроки могут возникать лейкозы, опухоли костной ткани.
Равномерно распределяющиеся радионуклиды НТО, 95Nb, 106Ru, 137Cs вызывают диффузную картину поражения с угнетением лимфопоэза, преимущественным возникновением опухолей молочных желез, гипофиза, яичников, почек, ЖКТ. При поступлении в организм гепатотропных радионуклидов 140La, 144Ce, 147Pm развиваются поражения слизистой оболочки желудка, кишечника, опухоли печени, скелета и желез внутренней секреции. В некоторых случаях биологическое действие радионуклидов зависит от пути их поступления в организм. Так, при введении через рот плохо резорбирующихся радионуклидов клиническая картина поражения характеризуется преобладанием местных процессов, связанных с избирательным отложением радионуклидов, с состоянием местной и общей реактивности организма.
Биологическое действие хорошо всасывающихся радиоактивных веществ не зависит от пути их введения в организм.
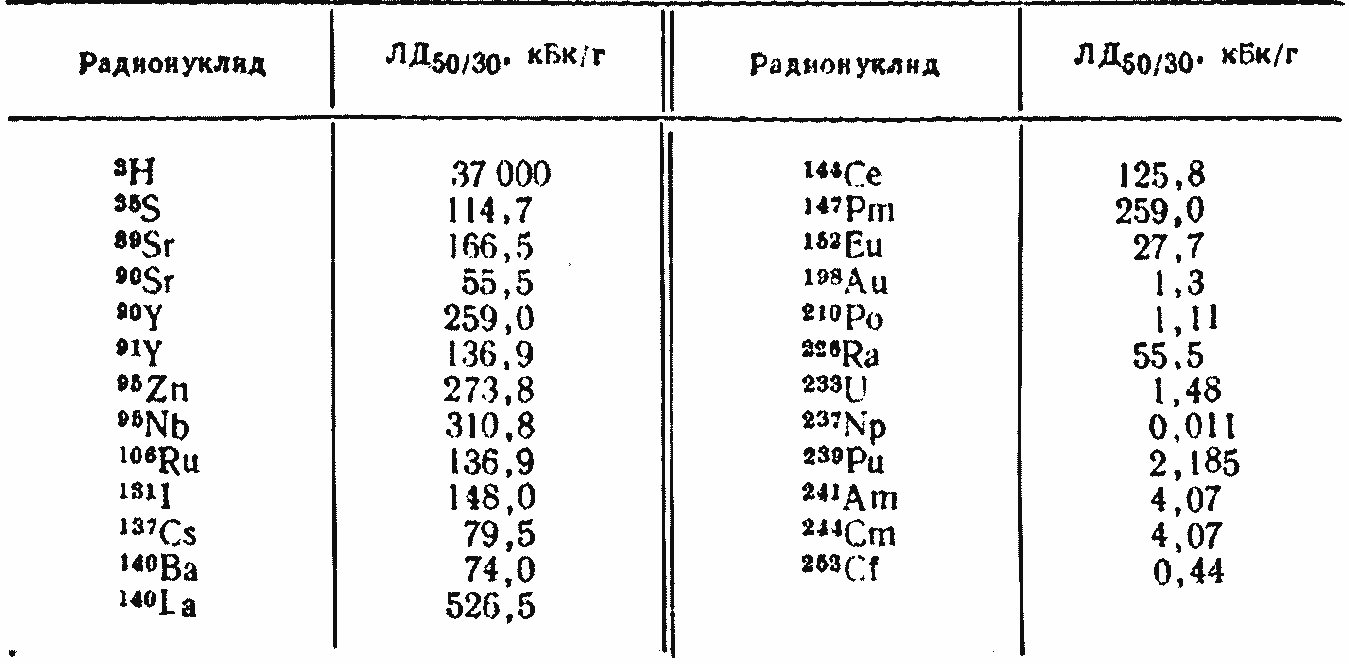
В токсикологической практике для оценки токсичности различных радионуклидов определяют летальные дозы. При изучении сравнительной токсичности различных радионуклидов пользуются абсолютно-летальной, минимально-летальной дозой и дозой, вызывающей гибель 50% животных к определенному сроку, например ЛД50/30 (табл. 1.7) [109].
Токсичность радионуклидов оценивают не по активности в беккерелях, а по поглощенной в организме тканевой дозе. При этом необходимо иметь в виду различную радиочувствительность органов и тканей на облучение и разную скорость восстановительных процессов.
Биологический эффект от инкорпорированных радионуклидов определяется поглощенной дозой в органах и тканях, кумулируемой за время пребывания их в организме.
Таблица 1.7. Дозы радиоактивных веществ, вызывающих гибель 50% крыс в течение 30 сут
Поглощенная доза D — это средняя энергия dE, переданная излучением веществу в некотором элементарном объеме, деленная на массу dm в этом объеме; D — dE/dm. Грей (Гр)—единица поглощенной дозы в системе единиц СИ: 1 Гр равен одному джоулю, поглощенному в килограмме вещества; 1 Г =1 Дж/кг=100 рад.
Радионуклиды с длительным периодом полувыведения из организма и большой энергией излучения создают высокие поглощенные дозы.
При оценке биологического действия радионуклидов важное значение имеет и мощность поглощенной дозы. Мощность поглощенной дозы Р — приращение поглощенной дозы dD за малый промежуток времени di, деленное на этот промежуток: Р— — DUdt. Эффективность облучения зависит от поглощенной дозы, а мощность поглощенной дозы оказывает влияние на формирование отдаленных эффектов, скорость восстановительных процессов. Биологическое действие радиоактивных веществ зависит не только от поглощенной дозы, но и от ее распределения во времени. Интенсивность облучения определяется ритмом поступления радионуклидов в организм, зависит также от чувствительности различных органов и систем и скорости репарации лучевых повреждений. Повреждающий эффект радионуклида при дробном введении проявляется в меньшей степени, чем при однократном введении в той же дозе. При дробном введении 2МPu в количестве 0,183—2,96 кБк/г увеличивается продолжительность жизни животных по сравнению с однократным введением [97]. Дробное введение 90Sr способствует увеличению продолжительности жизни крыс, уменьшает выход остеосарком.
При этом наблюдается менее выраженное угнетение лейко- и тромбопоэза по сравнению с однократным введением. Развитие у животных лейкозов и анемий не зависит от условий поступления радионуклида.
В результате длительного облучения организма при инкорпорации радионуклидов могут развиваться отдаленные последствия в виде опухолей разных органов и тканей, развития лейкозов и т. п. Отдаленные последствия могут возникать не только от попадания внутрь радиоактивных веществ, но и при действии на организм γ-излучения, нейтронов и протонов. Однако не во всех случаях в отдаленные сроки после поражения радиоактивными веществами развиваются злокачественные новообразования. Наблюдается патология со стороны отдельных органов и систем (уменьшение количества эритроцитов и лейкоцитов. развитие склеротических процессов, раннее старение организма).
После воздействия радионуклидов на организм животных наблюдается восстановление нарушенных функций отдельных органов и всего организма в целом. Процесс восстановления протекает в несколько этапов. Восстанавливаются внутриклеточные мембраны и структуры. Восстановительные процессы в условиях гипоксии происходят быстрее, нежели в обычных условиях. Считают, что процессы восстановления идут со скоростью, пропорциональной дозе облучения. Однократное действие γ-излучения на мышей в дозе 2,58· 10“' Кл/кг вызывает 100%-ную гибель животных к 22 сут. от лучевой болезни. Если мышей облучать в той же дозе, но дробно по 2,58-10-2 Кл/кг в сут, то погибает только 90% животных. Дробление дозы по 1,93 и 1,29-10-2 Кл/кг снижает смертность мышей на 35—45%. Эти данные свидетельствуют о том, что наряду с накоплением смертельной дозы происходит восстановление нарушенных функций организма. Наиболее выраженные процессы восстановления наблюдаются у мышей при дробном облучении в дозе 1.29·10-2 Кл/кг в течение 20 сут. В этом случае смертность животных от воздействия суммарной дозы 2,58-10-2 Кл/кг составила всего 35%. Известно, что при однократном облучении мыши погибают от воздействия дозы 11,32-10-2 Кл/кг и более.
При расчете дозы, вызывающей поражение, необходимо знать период полувосстановления. Это время, в течение которого нарушенные функции отдельных органов в облученном организме восстанавливаются ровно наполовину.
Н. А. Запольская и другие изучали восстановительные процессы в эпителии слизистой оболочки тонкого кишечника крыс при введении смеси радионуклидов. Смесь вводили ежедневно через зонд в желудок из расчета 55,5-104 Бк на крысу в течение 30 сут. Суммарная поглощенная доза на кишечник за период введения смеси радионуклидов составила 3,5 Гр.
Авторы установили, что период полувосстановления эпителиальных клеток крипт кишечника составлял примерно 23 сут. Следовательно, темп восстановления равен примерно 3% в сут. По данным Дэвидсона период полувосстановления у мышей, крыс, собак и ослов равен 3—8; 6—9; 14 — 18 и 20—28 сут. соответственно.
По теории Блера доза, вызывающая поражение при длительном облучении (например, от радиоактивных осадков), складывается из дозы, вызывающей необратимое поражение (около 10% всей накопленной дозы), и общей накопленной дозы с учетом репаративных процессов в организме (в среднем 12.5% в сутки). Период полувосстановления у человека равен 25-45 сут.
В Советском Союзе для обеспечения безопасности работы с радиоактивными веществами и источниками излучения приняты предельно допустимые дозы (ПДД) для повседневной работы. С внешними источниками излучения и радиоактивными веществами разрешается работать при дозе облучения профессионалов не более 0,05 Гр в год, а отдельных лиц из населения 0,005 Гр в год.
Оценивая биологическое действие радиоактивных веществ и источников ионизирующих излучений на организм, необходимо четко разграничивать соматические и генетические последствия облучения. Соматические эффекты, вызванные действием излучения, касаются лишь самого облученного организма, в то время как генетические эффекты (действие излучений на зародышевые клетки) в большинстве случаев не опасны для данного индивидуума, но могут оказаться опасными для последующих поколений. Однако, если в большей части зародышевых клеток в результате облучения возникнут летальные мутации, нарушится репродуктивная способность данного индивидуума; хотя физическое состояние его может и не отличаться от нормы, произойдут генетические изменения. Генетические изменения могут сочетаться с соматическими нарушениями.
При соблюдении правил работы и техники безопасности можно полностью избежать вредного воздействия радиоактивных веществ на организм человека.

