Стронций — щелочноземельный металл II группы Периодической системы Д. И. Менделеева. Порядковый номер 38, атомная масса 87,62, открыт в 1808 г. английским ученым Дэви. Название получил от минерала стронцианита. В настоящее время известно несколько изотопов (от 8lSr до 9?Sr). Наибольший интерес в токсикологии представляют изотопы 89Sr и 90Sr. Они образуются при облучении урана в ядерных реакторах, а также при взрывах атомных бомб как продукты ядерного деления.
90Sr — чистый β-излучатель с энергией β-частиц 0,54 МэВ и периодом полураспада 28,6 г. Дочерним продуктом распада 90Sr является 90Y, который находится вместе с ним в равновесном состоянии. Период полураспада 9ηΥ составляет 64,2 ч, максимальная энергия β-частиц 2,18 МэВ. 89Sr также β-излучатель. Период полураспада его 53 сут, энергия β-частиц— 1,5 МэВ [13].
Стронций—стабильный микроэлемент, постоянно присутствующий в тканях и органах человека и животных. Содержание Sr в земной коре составляет около 0,04%. Встречается он в виде силикатных пород и труднорастворимых углекислых солей. Он входит в состав мела, извести, гипса, мрамора. Металлический стронции — металл серебристо-белого цвета.
Стронций является аналогом кальция. При поступлении в организм, так же как и Са, включается в минеральный обмен. Соединения Sr растворимы в воде. Он хорошо окисляется, с водой образует гидроксиды, являющиеся сильными основаниями. Окисление его с галоидами идет с выделением тепла.
Распределение стронция в биосфере крайне неравномерное. Он в значительно больших количествах содержится в морской воде и морских организмах, чем в пресноводных водоемах [16]. В органах и тканях живого организма содержание Sr составляет от 0,01 до 0,1 мкг на 1 г свежей ткани. В скелете рыб, животных, раковинах моллюсков содержится до 95—99% Sr, содержащегося во всем организме.
Таблица 5.1. Всасывание стронция в ЖКТ

При выпадениях на поверхность земли 90Sr мигрирует по биологическим цепочкам и с продуктами растительного и животного происхождения может попадать в организм человека. При поступлении внутрь организма 90Sr, так же как и Са, хорошо всасывается в ЖКТ, значительные количества его откладываются в скелете. Это приводит к облучению не только костей и костного мозга, но и других тканей вследствие воздействия β-излучения 90Sr и его дочернего продукта 90Y.
Уровни всасывания стронция в ЖКТ колеблются в очень широких пределах и зависят от многих факторов. Важное значение при резорбции стронция из кишечника имеют диета, физико-химические свойства соединения, возраст животных и человека и функциональное состояние организма. В табл. 5.1 приведены данные различных авторов по влиянию возраста и содержания Са в диете на всасывание стронция в ЖКТ. Как видно из таблицы, всасывание Sr из ЖКТ колеблется от 5 до 100%· У взрослых мышей всасывание составляет от 60 до 80%, у крыс в зависимости от возраста — от 25 до 100%. Всасывание Sr у кроликов и собак не превышает 14—25% [117].
По данным Линески резорбция Sr из кишечника людей составляет от 11 до 99 %. Значительно большее всасывание стронция из кишечника молодых животных связано с более высокой потребностью организма в щелочноземельных элементах, необходимых для построения скелета.
Существенно влияет на резорбцию Sr из кишечника проницаемость стенки ЖКТ. В работе Б. А. Анненкова показано, что на всасывание Sr в кишечнике существенно влияет Са. Так, при увеличении содержания Са в диете задержка Sr в организме снижается. Однако Ворман и другие считают, что эта закономерность существует лишь в определенном возрасте. Добавка Са к рациону эффективна только для молодых животных, а для взрослых и старых животных не имеет существенного значения. Авторы считают, что происходит разбавление радиоактивного изотопа стабильным, что и способствует меньшему всасыванию Sr в кишечнике. Нам представляется механизм всасывания стронция под влиянием кальция гораздо сложнее, так как уменьшение всасывания зависит также и от содержания фосфора в диете. Этот процесс зависит и от других факторов: введение в организм стронция с молоком увеличивает всасывание изотопа не только у молодых, но и у пожилых людей (см. табл. 5.1).
Таким образом, всасывание Sr в кишечнике — пассивный диффузионный процесс, который зависит от физико-химических и физиологических факторов: возраста, характера питания, состояния минерального обмена, скорости продвижения химуса по пищеварительному тракту, беременности [13].
При поступлении изотопов Sr через кожу в количестве 24,05· 104 Бк/смг процесс фиксации их происходит сразу же после загрязнения кожной поверхности. Основное количество (73—85%) проникших в кожу изотопов приходится на нерастворимые в воде белковые и неорганические ингредиенты остаточной фракции, около 11% связывается с жирорастворимыми веществами и 6—17% переходит в водные экстракты [111]. По данным Л. Н. Будко всасывание 90Sr в количестве 18,5Х105 Бк через неповрежденную кожу крыс за 6 ч составляет 0,3% нанесенного количества. Через 12 сут. в скелете крыс его содержится до 4%.
Важное практическое значение имеет поступление 90Sr через органы дыхания. В экспериментах на крысах Г. К. Королевым [62] установлено, что 90Sr быстро всасывается из легких. Через 5 мин после интратрахеального введения в дозе 1.48Х104 Бк/г в легких остается 33,3% введенного количества, а через 1 сут. всего 0,39%.
Путь поступления изотопов Sr в организм существенно влияет на отложение в скелете (табл. 5.2).
Таблица 52. Депонирование 14Sr в скелете при различных путях поступления в организм (% введенного количества)
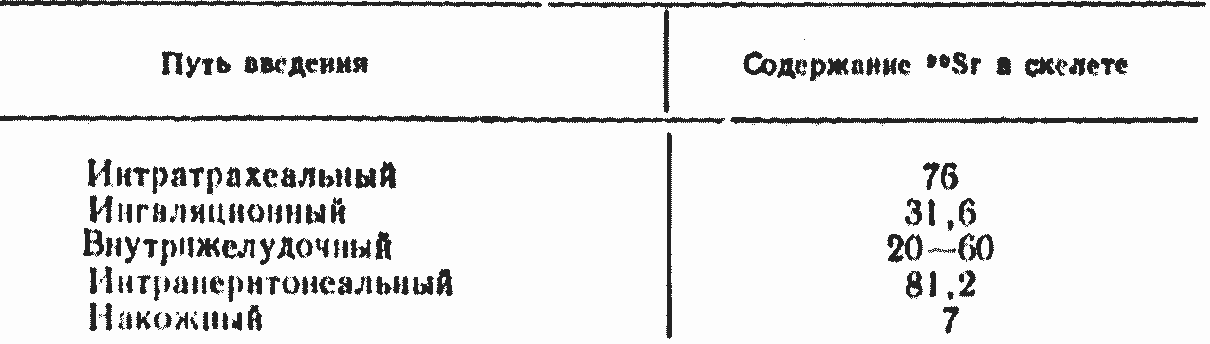
Из таблицы видно, что наибольшие количества 90Sr откладываются в скелете при интраперитонеальном и интратрахеальном введении в организм. При ингаляционном поступлении депонирование 90Sr в скелете почти в 2,5 раза меньше, чем при интратрахеальном введении. По-видимому, заглатывание большого количества изотопа при ингаляции значительно снижает всасывание его в легких. Наименьшие количества 90Sr всасываются при внутрижелудочном и накожном поступлении.
Изотопы Sr имеют скелетный тип распределения. При любом пути поступления в организм они избирательно откладываются в костях. Депонирование Sr в мягких тканях составляет не более 1%. Материалы исследований Л. А. Булдакова и Ю. И. Москалева [13], проведенных на крысах и собаках при однократном внутрибрюшинном введении 90Sr, свидетельствуют о том, что через 30 мин в костях 45-суточных крыс 90Sr почти в 3,5 раза больше (67,3%), чем у старых животных (19,45%). В мягких тканях, наоборот, у старых животных 90Sr откладывается в несколько большем количестве, чем у молодых. Величина депонирования 90Sr в скелете собак в зависимости от возраста при пероральном введении колеблется от 19,7 до 71,5%. Вероятно, уменьшение степени задержки радионуклидов в скелете с увеличением возраста связано с уменьшением доли 90Sr, которая прочно фиксируется в скелете.
Несмотря на низкое содержание 90Sr в мягких тканях и избирательное отложение его в скелете, авторы отмечают некоторые различия в распределении радионуклида по органам. Так, через 1 сут. после внутривенного введения 90Sr в дозе 7,4· 105 Бк на животное наиболее высокая концентрация его у крыс обнаруживается в почках (0,28% на I г сырой массы), слюнной (0,09%) и щитовидной (0,07%) железах, наиболее низкая — в костном мозге, надпочечниках и шкурке (по 0,001%). Наиболее низкая концентрация 90Sr у собак наблюдается в мышцах, коже и головном мозге.
Большинство исследователей считают, что распределение изотопов Sr в различных частях одной и той же кости и разных костях скелета неравномерное. Так, по данным 10. И. Москалева [74] в начальные сроки концентрации Sr в эпифизе и метафизе у крыс в 2,5 раза выше, чем в диафизе. У собак более высокое его содержание оказывается в метафизе бедра (до 90% в 100 г кости ко вторым суткам), в эпифизе (33%) и ребрах (62%). Самая низкая концентрация стронция обнаружена в костях черепа и зубах (5—8%). Эти данные свидетельствуют о том, что стронций откладывается в участках костей, обладающих наибольшей зоной роста.
Георге и другие изучали накопление и выведение 90Sr из костей животных. Кроликам подкожно вводили 3,7·101 Бк 90Sr и забивали их на I. 15 и 100 сут. после введения. Определяли содержание 9flSr в костях и тканях. Установлено, что через 24 ч после введения 90Sr в 100 мл крови содержался 1% радионуклида, к 15 сут. —0,01%.
Содержание 90Sr в мягких тканях составляло 10 и 1% введенного количества на 1 и 15 сут. соответственно. Содержание 90Sr в скелете повышалось до 23,3% на 15 сут. после введения. В исследованиях in vitro показано, что смесь глюконата кальция и кальциферола наиболее эффективна при удалении 90Sr из кости. В исследованиях in vivo показано, что использование комплекса кальций — витамин Д приводило к удалению 75 и 45% 90Sr из кости на 1 и 4 сут. после введения изотопа.
Микрораспределение Sr в костях по данным авторадиографических исследований указывает на сравнительно равномерное распределение его в минеральной части кости. Стронций концентрируется под эпифизарным хрящом, под эндостом в метафизарной области и под периостом в середине стволовой части кости, т. е. в тех участках, где происходит активное образование кости [168].
При повторном и длительном поступлении Sr в организм характер распределения его такой же, как и при однократном введении, наибольшее количество радионуклида обнаруживается в костной ткани. По данным Л. А. Булдакова у крыс через 140—365 сут. после суточного перорального введения 90Sr в дозе 1,48·104 Бк содержание в скелете составило 32—36% ежедневно вводимого количества. Содержание стронция в 1 г сырой массы в ткани печени — 1,6—1,49%, в мышцах 0,05— 0,11, в почках 0,01—0,07%. Количество Sr в костях остается значительно выше и после прекращения поступления радионуклида в организм. Авторы отмечают, что в условиях длительного поступления в организм наиболее высокие концентрации 90Sr у собак обнаруживаются в бедре, зубах, теменной кости, нижней челюсти.
Таким образом, приведенные данные свидетельствуют о том, что независимо от пути и ритма поступления стронция в организм, основные количества его депонируются в скелете. Отложение стронция в скелете зависит от интенсивности обменных процессов. При повышении обменных процессов уменьшается отложение и ускоряется выведение его из организма. Замедление обмена веществ способствует большему отложению в организме [119]. Беременность и лактация способствуют меньшему отложению Sr в организме самок крыс. По данным В. Г. Куликовой через 2 сут. после внутрибрюшинного введения Sr в скелете контрольных животных задерживается 31,3%, а у лактировавших самок степень задержки уменьшается до 12,9%.
Таблица 5.3. Выведение стронция из организма животных и человека
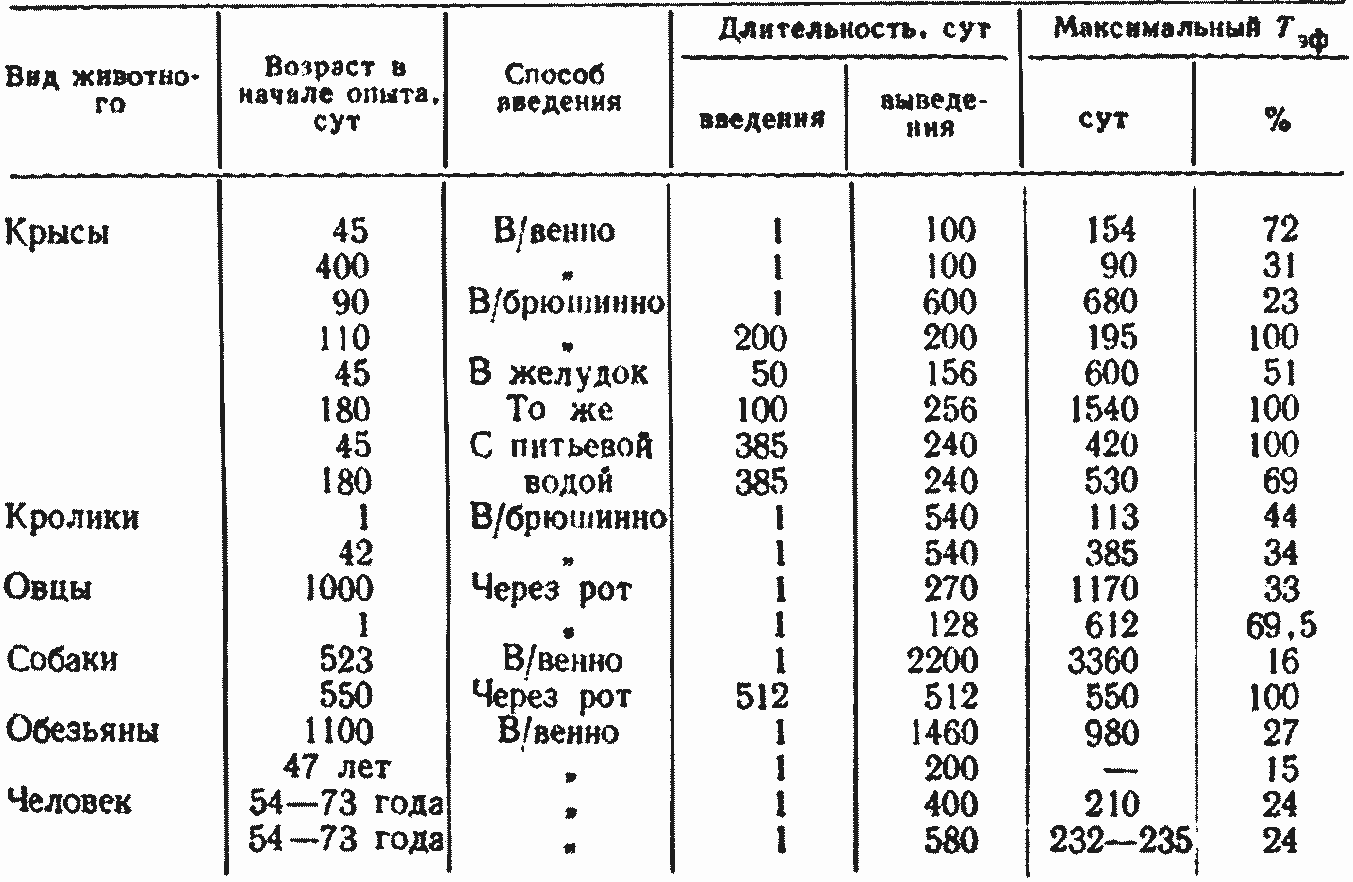
Выделение стронция из организма происходит с калом и мочой. При пероральном поступлении большая часть радионуклидов выделяется с калом, при ингаляционном — с мочой. В исследованиях Ю. И. Москалева [74] при введении 90Sr крысам в лозе 1,48-10* Бк показано, что 63% стронция из скелета выводится с Тб равным 65 сут. и 37% с Тб равным 680 сут. В отдаленные сроки после внутрибрюшинного введения стронция радиоактивность мягких тканей на 3—4 порядка ниже радиоактивности скелета. В соответствии с этим некоторыми авторами установлено несколько периодов полувыведения стронция из организма. Короткие периоды полувыведения (2,5—8,5 сут) характеризуют выведение стронция из мягких тканей, длинные периоды (90—154 сут) — преимущественно выведение из костей [74].
Важное практическое значение имеют данные о выделении стронция при хроническом поступлении в организм. В опытах на собаках Д. И. Ильиным показано, что после длительного перорального введения 90Sr в дозе 1,11-104 Бк период полувыведения его из скелета составляет 200 сут. Различие в периодах выведения стронция после однократного и длительного поступления радионуклида объясняется тем, что при длительном введении в организм относительная величина быстро выводящейся фракции уменьшается, а значение доли Sr, прочно фиксированного в скелете, резко возрастает (табл. 5.3).
В экспериментах на животных установлено, что 9<lSr выделяется также с молоком. Поступление его в молоко зависит от способа введения изотопа и не зависит от его дозы. При пероральном введении количество стронция в молоке в 8—10 раз ниже, чем после внутрибрюшинного или внутривенного введения [13].
Таблица 5.4. Токсичность 90Sr для крыс

Многочисленные исследования отечественных и иностранных авторов посвящены изучению биологического действия Sr [130, 142].
В табл. 5.4 приведены данные о токсичности Sr для крыс при различных путях введения в организм. Наиболее токсичен стронций при внутрибрюшинном введении. Так, ЛД50/30 составляет 43,8· 106 Бк/кг, а ЛД50/30 при введении под кожу равна 74·107 Бк/кг. Наибольшая продолжительность жизни крыс отмечена при введении Sr в дозе 1,85· 10s Бк/кг. Она составила 407 сут.
Н. Г. Яковлева однократно вводила крысам 90Sr и 45Са в количествах 92,5· 102 и 4,81 · 104 Бк/г и хронически ежедневно в течение года — в количествах 1,48 и 4,44· 104 Бк на крысу. После однократного введения 90Sr и 45Са отчетливо проявлялось угнетение лейкопоэза (поглощенные дозы в костной ткани 20—30 Гр за первые 3 мес). Лейкопения достигала максимума к 7— 14 сут. и была глубокой при введении только 90Sr. При введении кальция она была неглубокой, к 30 сут. количество лейкоцитов нормализовалось. Тромбоцитопения раньше развивалась при введении 90Sr. Максимальное снижение тромбоцитов отмечалось на 14 сут. и в дальнейшем не восстанавливалось. При однократном введении 90Sr и 45Са через 14 сут. увеличивалось число аномальных лейкоцитов, которое превышало данные контроля в 5 и 2,3 раза соответственно. При сравнении однократного и хронического действия 90Sr и 45Са отмечается, что в отдаленные сроки относительный эффект снижения форменных элементов крови при хроническом облучении выражен сильнее, чем при однократном воздействии.
Благодаря специфике отложения 90Sr создаются такие условия, когда облучается не весь организм, а преимущественно скелет и костный мозг. Поэтому наиболее выраженные изменения при поражении стронцием возникают в этих органах. Введение крысам остроэффективной дозы 90Sr (2,78—11,1 Бк/г) вызывает выраженные изменения в периферической крови: лейкопению, лимфопению, нейтропению, ретикулопению. Снижается также количество гемоглобина и число эритроцитов [62].
У животных развивается типичная картина острой лучевой болезни. Подострое течение болезни характеризуется постепенным развитием анемии. Снижается не только количество клеток в периферической крови, но происходит резкое уменьшение и костномозговых клеток.
Меньшая доза 9flSr (0,074 Бк/г), не вызывающая значительного укорочения продолжительности жизни, существенно влияет на сперматогенез и овогенез, состояние функции печени и почек, иммунологическую реактивность и нейроэндокринную систему [13, 62, 117, 142].
Патоморфологическая картина поражения 90Sr характеризуется уменьшением лимфоидных элементов в селезенке и лимфатических узлах, наличием очагов некрозов в печени. В головном мозге — периваскулярный отек, единичные кровоизлияния в коре. В почках — нерезко выраженные явления нефроза [130].
Результаты экспериментальных исследований показывают, что биологическое действие стронция весьма многообразно. В отдаленные сроки после поражения, как при однократном, так и длительном поступлении изотопа, у животных развиваются лейкозы и опухоли костей. Проведенные Η. Н. Литвиновым исследования [69] свидетельствуют, что злокачественное перерождение костных клеток возникает при сравнительно небольших уровнях воздействия 90Sr (1,85· 104 Бк/г) и мало зависит от фактора времени, т. е. от ритма воздействия радионуклида, и проявляется после накопления определенной пороговой дозы излучения. При поражении 90Sr у подопытных крыс частота лейкозов в 2—4 раза больше, чем у контрольных животных [130].
Наряду с остеосаркомами в отдаленные сроки при воздействии 90Sr развиваются новообразования желез внутренней секреции, опухоли гипофиза, молочных желез, яичников и других тканей. В литературе имеются сведения о профилактических и терапевтических средствах при поражении 90Sr. Одним из принципов терапии поражений радиоактивными веществами являются мероприятия по скорейшему удалению изотопа из организма, а также использование замещающих средств, комплексообразователей и средств, влияющих на обмен веществ.
Неотложная помощь при поражении изотопами Sr.
Дезак тивация открытых участков кожи 5%-ным раствором пентацина, 2%-ным раствором HCI, препаратом «Защита-7», моющими порошками «Эра» или «Acтра», пастой НЭДЭ. Внутрь — адсорбар или BaSO4, 25,0:200,0; полисурьмин 4,0:200,0. Назначение рвотных средств: 1%-ный апоморфин — 0,5 мл.
Обильное промывание желудка. После очищения желудка повторное назначение указанных сорбентов с солевыми слабительными. Внутривенно 10%-ный СаCl2—10 мл. Внутрь уродан — 1 чайная ложка на стакан воды 3 раза в день, эуфиллин 0,15 г. При ингаляционном поступлении пылевидных препаратов обильное промывание носа и полости рта. Отхаркивающие: термопсис с содой. Мочегонные: гипотиазид 0,2 г, фонурит 0,25 г [79].
При нормировании изотопов Sr необходимо учитывать, чтобы ежедневно поступающие количества его при ингаляции, с водой и пищей не превышал и ПДС изотопа в скелете человека в период всей его жизни.
ПДП для персонала через органы дыхания для 90Sr составляет 51,8-104 Бк/год, ДК для 90Sr в воздухе рабочих помещений 4,44-10'2 Бк/л, в атмосферном воздухе 14,8-10-4 Бк/л, в воде — 14,8 Бк/л.

