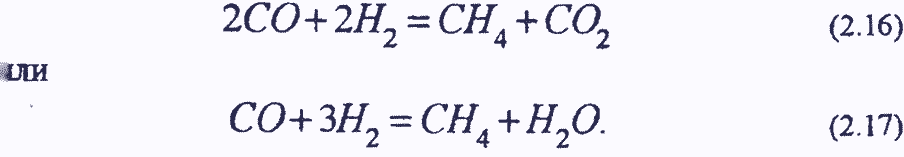Комплексоны широко применяются в теплоэнергетике. Наиболее распространены этилендиаминтетрауксусная кислота (ЭДТА)
![]()
и ее соли. Из солей наибольшее применение в теплоэнергетике нашла двузамещенная соль ЭДТА - трилон Б. Зарубежные фирмы ЭДТА и ее солям дают различные наименования: секверстрен, комплексон - П, титриплекс-П, версен, вертан, секверстол, селектрон Б и т.д.
Соединения, образуемые комплексонами, получили наименование “клешневидных” или “хелатосоединений”. Диссоциация этих соединений идет в первую очередь по внешней сфере, затем по внутренней. Комплексы, образуемые ЭДТА и ее солями, очень устойчивы. Растворимость ЭДТА невелика, значительно выше растворимость ее солей, что видно из табл. 2.3 [32].
Таблица 2.3 Растворимость ЭДТА, г/л, и ее натриевых солей в воде при различных температурах и pH растворов при комнатной температуре
Комплексон | Температура | pH | ||
22 | 40 | 80 |
| |
ЭДТА | 2 | 2 | 5 | 1,0 |
Однозамешенная соль ЭДТА | 14 | 14 | 21 | 3,5 |
Двузамещенная соль ЭДТА (трилон Б) | 108 | 137 | 236 | 5,5 |
Трехзамещенная соль ЭДТА | 465 | 465 | 465 | 8,0 |
Четырехзамещенная соль ЭДТА | 600 | 590 | 610 | 10,5 |
С ЭДТА двухвалентное железо образует три пятичленных цикла, а трехвалентное железо - четыре пятичленных цикла.

Для других катионов имеются аналогичные комплексные соединения. Так медь, латунь уже при температурах до 100 °C энергично связываются в комплексы с ЭДТА и ее солями.
Термическая диссоциация ЭДТА начинается при температуре 140, а ее солей - при 16О°С. Степень диссоциации солей несколько меньше, чем ЭДТА, и в пределах концентрации до 1000 мг/л не зависит от концентрации раствора.
Для полной термической диссоциации ЭДТА и ее солей достаточно образования аминов и других продуктов термолиза; в газовую фазу переходят СО7, H2, СО, СH4, CH2O [20].
Соединения, образующиеся при термолизе комплексонов, обладают более высокой комплексообразующей способностью, чем исходные соединения, и с ростом температуры процесс комплексообразования ускоряется. Образующиеся комплексонаты железа при температурах выше 250 С термически более устойчивы, чем комплексоны, но и они при 290 С и выше подвергаются практически полному термическому разложению. Термически наиболее устойчивыми являются комплексонаты кальция и магния, до температуры 370X2 они практически не разлагаются.
Термолиз комплексонатов железа при температуре выше 290°С протекает с образованием магнетита, который в условиях контакта с поверхностью металла образует на ней плотную защитную пленку.
В продуктах разложения комплексонатов обнаружены водород, метан и оксид углерода, максимальная концентрация которых наблюдается в свежем или вторичном паре. В турбинном конденсате эти газы не обнаруживаются, так как они отсасываются эжектором из парового пространства конденсатора. Рост концентрации водорода и оксида углерода прямо пропорционален дозе комплексона.
В свежем паре обнаруживается метан, предположительно образующийся по реакциям: