ГЛАВА ВТОРАЯ
2. ХИМИЧЕСКИЕ РЕАГЕНТЫ, ПРИМЕНЯЕМЫЕ ПРИ КОНСЕРВАЦИИ ОБОРУДОВАНИЯ
2.1. ГИДРАЗИН
2.1.1. Химические и физические свойства гидразина
Гидразингидрат![]() - бесцветная жидкость, легко поглощает воду, углекислоту и кислород из воздуха. Гидразингидрат хорошо растворим в воде и спирте. Температура кипения при атмосферном давлении + 118,5°С, замерзания -51,7X3. Молекулярная масса реагента равна 50, плотность 1,03 г/см3. Гидразингидрат обладает сильными восстановительными свойствами, токсичен, а при концентрациях, превышающих 40 %, горюч. Основной метод получения гидразингидрата в производственных масштабах - это использование синтеза Рашига, включающего частичное окисление аммиака (и мочевины) гипохлоритом.
- бесцветная жидкость, легко поглощает воду, углекислоту и кислород из воздуха. Гидразингидрат хорошо растворим в воде и спирте. Температура кипения при атмосферном давлении + 118,5°С, замерзания -51,7X3. Молекулярная масса реагента равна 50, плотность 1,03 г/см3. Гидразингидрат обладает сильными восстановительными свойствами, токсичен, а при концентрациях, превышающих 40 %, горюч. Основной метод получения гидразингидрата в производственных масштабах - это использование синтеза Рашига, включающего частичное окисление аммиака (и мочевины) гипохлоритом.
Для гидразингидрата предполагается, что в жидкой фазе существует равновесие
![]() (2-1)
(2-1)
которое с увеличением температуры смещается вправо [34]. Реакция между гидразином и водой протекает с образованием иона гидразония ![]() :
: ![]() (2-2)
(2-2)
Растворы гидразина в воде обладают основными свойствами. Как основание он в 8 раз слабее гидрооксида, и его можно рассматривать как аммиак, в котором один атом водорода замещен группой NH. С кислотами гидразин образует соли, которые в воде разлагаются по реакции
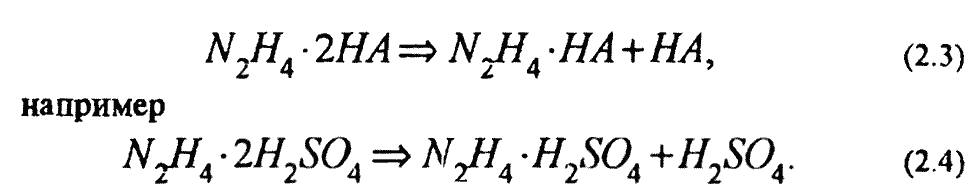
Гидразин способен выступать в качестве донора пары электронов при образовании комплексов с ионами металлов, что связано с возможностью гидразина координационно присоединять ион водорода с образованием иона Ν2Η4-Н+. При образовании таких гидразинатов гидразин ведет себя главным образом как координационно-двухвалентная молекула и действует в воде в качестве восстановителя металлов.
Гидразин как в кислой, так и в щелочной среде подвергается реакции самоокисления - восстановления
![]() (2.5)
(2.5)
Продуктами реакции трехвалентного железа и гидразина являются азот и аммиак:
![]() (2-6)
(2-6)
2.1.2. Комплексные соединения гидразина. Термическая устойчивость гидразина.
Как отмечалось выше, гидразин способен выступать в качестве донора пары электронов с образованием ионов гидразония.![]() , хотя
, хотя
в большинстве случаев координационно связанный с ионами металлов гидразин ведет себя как координационно-двухвалентная молекула, возможно существование и трехчленных металл-гидразиновых
колец типа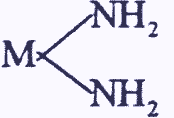 , а также моногидразинатов:
, а также моногидразинатов:
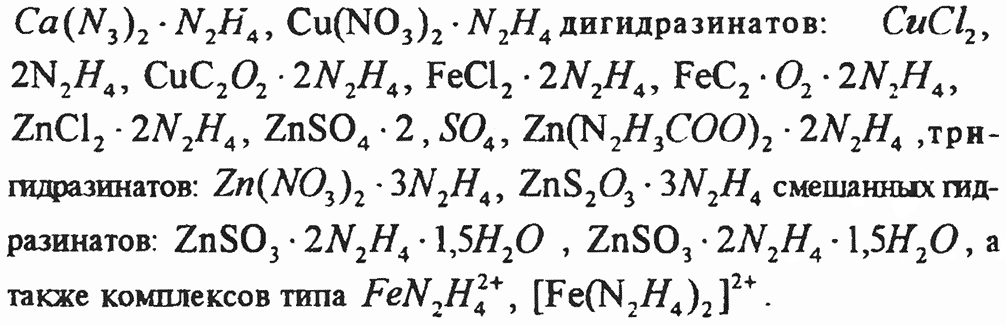
Многие соединения, содержащие координационно-связанный гидразин, слабо растворимы в воде, и вполне возможно, что некоторые из них представляют собой поликатионные комплексы, в которых гидразин является мостиковой группой. Число возможных соединений с координационным гидразином несколько ограничено вследствие его восстанавливающей способности.
Добавление гидразинов даже к водным растворам солей металлов приводит к осаждению нерастворимых комплексов.
При повышенных температурах гидразин разлагается с образованием аммиака и азота

При температурах выше 100°С также достаточно интенсивно протекают реакции
(2.7)
(2.8)
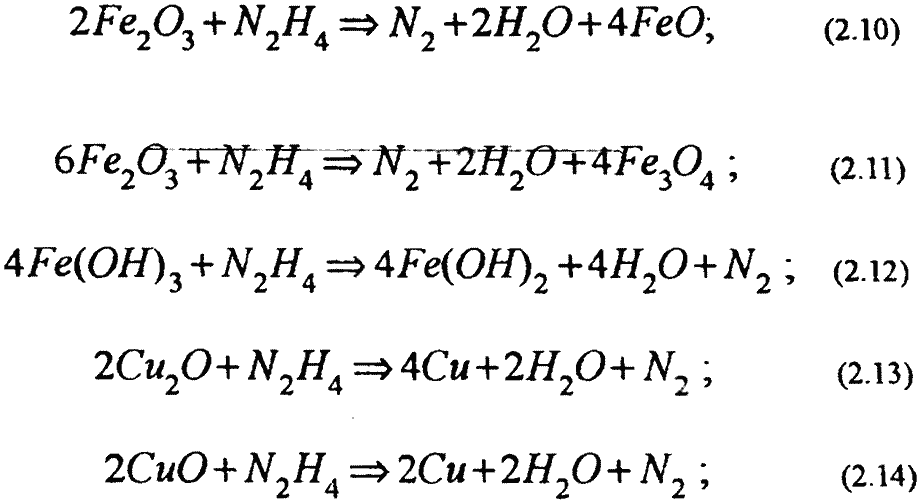
Скорость термического разложения гидразина зависит от pH раствора. Так, при pH менее 8 и температуре 300 С разложение гидразина происходит через 10 мин, а при pH 8 и 9 (и той же температуре) - соответственно через 20 и 30 мин.
Катализаторами температурного распада гидразина являются оксиды железа, меди и других металлов. На разложение гидразина влияет также состояние стенок трубок, в которых циркулирует раствор. При движении растворов каталитическое воздействие стенок труб сказывается достаточно сильно. В неподвижном растворе скорость термолиза гидразина замедляется. С увеличением давления скорость разложения гидразина также уменьшается. Гидразин способен переходить в пар лишь при насыщении системы. Скорость его разложения в паре зависит в первую очередь от температуры.
Авторы обнаружили в паре 0,5-0,7 мг/кг гидразина на котлах давления 3,5 МПа при температуре перегрева 430 С и 0,3 мг/кг при давлении 17,0 МПа и температуре перегрева 510 С.
Влияние температуры на взаимодействие гидразина и кислорода.
В отсутствие катализаторов pH незначительно влияет на скорость окисления гидразина. Гораздо большее влияние на этот процесс оказывает температура. Автором проводилось исследование скорости взаимодействия кислорода и гидразина при различных температурах и значениях pH [25].
Эксперименты ставились таким образом, чтобы реакция проходила либо при близких по значению концентрациях взаимодействующих веществ (бимолекулярная реакция), либо при постоянном и значительном избытке одного из компонентов (мономолекулярная реакция). Значение pH поддерживалось постоянным с помощью универсальной буферной смеси; для сохранения постоянства температуры растворы термостатировались. Результаты проведенных исследований представлены на рис. 2.1. Пучок кривых характеризует изменение константы скорости исследуемой реакции в зависимости от температуры при различных pH. Кривые лежат настолько близко друг к другу, что их можно рассматривать как одну и считать, что скорость окисления гидразина кислородом в пределах pH 8,5-12 зависит только от температуры При математической обработке полученных кривых можно вывести формулу, позволяющую рассчитывать количество непрореагировавших компонентов при различных температурах и разном времени контакта. Результаты подсчетов приведены в табл. 2.1.
Таблиц а 2.1 Количество непрореагировавшего компонента в зависимости от времени контакта, %
Время, мин. | Температура, град. | |||||||
20 | 40 | 70 | 100 | 120 | 150 | 200 | 250 | |
1 | 99,97 | 99,96 | 99,72 | 98,50 | 95,98 | 85,90 | 39,19 | 1,67 |
2 | 99,97 | 99,93 | 99,45 | 97,03 | 92,13 | 73,79 | 15,36 | 0,028 |
5 | 99,95 | 99,82 | 98,65 | 93,26 | 81,49 | 49,52 | 0,93 | 13-10-8 |
Из приведенных данных видно, что заметное взаимодействие реагирующих веществ начинается только при 150 C при этой температуре, если реакция протекает по мономолекулярному механизму, за 5 мин. может быть связано до 50% меньшего по количеству компонента. При 250X3 почти 100% его будет связано за 1 минуту. Если же концентрации гидразина и кислорода близки, как, например, в питательной воде, реакция проходит по бимолекулярному механизму. Подсчеты, проведенные для концентрации гидразина 0,03 и кислорода 0,02 мг/л представленные в табл. 2.2.
Таблица 2.2 Количество гидразина, вступившего в реакцию с кислородом, %
Время, мин. | Температура, | |
200 | 250 | |
1 | 0,43 | 7,10 |
2 | 3,30 | 13,30 |
5 | 9,00 | 26,60 |
Эти данные показывают, что даже при температуре 250 С через 5 мин остается несвязанным свыше 70% гидразина (из 30 мкг гидразина и 20 мкг кислорода прореагировало только по 8 мкг). При более низких температурах реакция идет значительно медленнее, что и объясняет их совместное сосуществование в питательной воде.
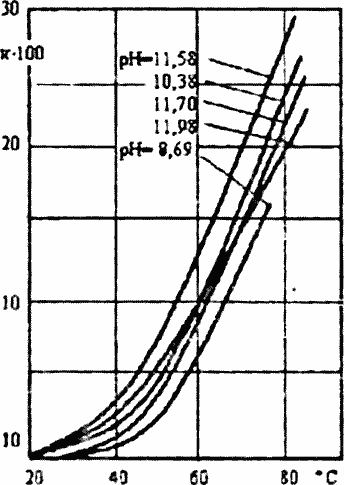
Рис. 2.1.3ависимость константы скорости взаимодействия кислорода с гидразинам от температуры при различных pH

