1.2. Влияние примесей на коррозию металлов в водной среде
На скорость и характер коррозии металла влияют как внутренние факторы - состав, гетерогенность, механические напряжения металла, так и внешние. Одним из решающих внешних факторов следует считать влияние на процессы коррозии присутствующих в воде различных химических соединений.
Так, анионы С1 , Вr, I мало влияют на кинетику анодного растворения металла в активной области коррозионного процесса и даже несколько тормозят реакцию. В пассивной области эти анионы часто вызывают депассивацию, и локальную коррозию металла. Депассивирующее действие галогенов имеет адсорбционную природу. Механизм депассивации объясняется адсорбцией хлор-ионов пассивной пленкой, из которой соответственно вытесняются и замещаются ионы кислорода. При этом получаются растворимые хлористые соединения металла и на участках металлической поверхности образуются поры [2].
Аустенитные нержавеющие стали способны пассивироваться в растворах и в присутствии хлоридов, но с увеличением концентрации последних область пассивного состояния уменьшается. В растворе хлоридов при отсутствии кислорода аустенитная сталь не подвергается коррозионному растворению, а с введением кислорода она корродирует тем быстрее, чем выше его концентрация в растворе При температуре 250-300 С коррозионное растрескивание аустенитных сталей наступает уже при содержании в воде хлорилов и кислорода более 0,5 мг/кт каждого.
В слабокислых растворах при наличии хлор-иона возникает точечная коррозия нержавеющих аустенитных сталей, развивающаяся не на границах зерен, а в отдельных точках поверхности и распространяющаяся со временем вглубь. Этот вид коррозии наблюдается для металла, находящегося на границе пассивного состояния, когда защитная пленка еще не обладает достаточной прочностью. Ослабленными частями поверхности могут быть отдельные включения оксидов реагирующих элементов, неровности поверхности, места, где защитная оксидная пленка еще только зарождается, и др.
Для развития точечной электрохимической коррозии в этом случае необходимо чтобы работала коррозионная пара анод-катод. Устойчивая работа такой пары возможна, если возникающий точечный анод в данных условиях не пассивируется под действием анодного тока. Это обеспечивается, например, наличием в растворе активных ионов хлора с одновременным присутствием кислорода или другого окислителя при слабокислой среде. В результате протекания анодного процесса на дне язвинки образуются вторичные гидрооксидные продукты коррозии, снижающие pH раствора. Скорость коррозии в глубину увеличивается из-за малых площадей анода и больших площадей катодных участков.
Высокая степень перехода продуктов коррозии в хлоросодержащую воду определяется уменьшением концентрации ионов Fe2+, преобразующихся в комплексное соединение трехвалентного железа по реакции
![]() (15)
(15)
Однако введение в раствор посторонних ионов может подавить депассивацию галогенами за счет их вытеснения из пассивной оксидной пленки.
Поданным [41] существует определенное соотношение концентраций посторонних анионов и хлоридов![]() , при котором язвенная коррозия подавляется. Значения а для различных анионов при рН=7 приведены ниже:
, при котором язвенная коррозия подавляется. Значения а для различных анионов при рН=7 приведены ниже:
![]()
При совместном воздействии кислорода пассивное состояние
стали нарушается значительно легче в кислом электролите, чем нейтральном. Пассивирующие свойства электролита, содержащего анион![]() , сильнее проявляются в кислом и щелочном растворе, чем в нейтральном. Так, авторы [41} дают определенные соотношения сульфатов и хлор-ионов, при которых депассивирующее действие на металл хлор-ионов прекращается.
, сильнее проявляются в кислом и щелочном растворе, чем в нейтральном. Так, авторы [41} дают определенные соотношения сульфатов и хлор-ионов, при которых депассивирующее действие на металл хлор-ионов прекращается.
Значения а для иона ![]() при различных pH приведены ниже:
при различных pH приведены ниже:
![]()
С вводом кислорода, например до 200 мг/кг, в нейтральной среде, содержащей хлориды, скорость коррозии стали повышается в 2 раза.
Нитриты выполняют двойственную роль при коррозии металла. С одной стороны, они служат мощным деполяризатором катодных участков коррозионных пар, ускоряя процессы электрохимической коррозии, с другой, нитриты, обладая окислительными свойствами, окисляют металл, создавая защитные оксидные пленки. Чем выше концентрация нитритов в растворе, тем больше вероятность образования защитных пленок.
Процесс нитритной коррозии металла можно охарактеризовать следующими реакциями:
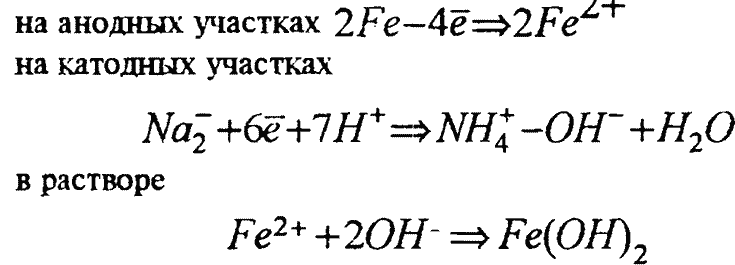 (16)
(16)
При повышенных температурах предполагается, что коррозия металла обуславливается и кислородом, образующимся в результате термического разложения нитритов по реакции:
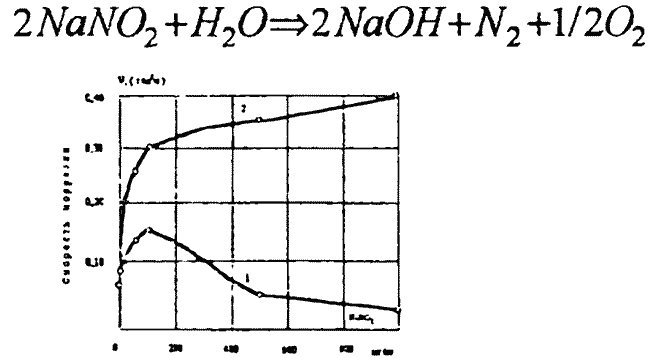
Рис. 1.3. Зависимость скорости коррозии стали от концентрации нитритов в котловой воде: 1,2 - при р, равном 3 и 10 МПа
Так, при давлении 3 МПа коррозионные свойства нитритов возрастают с ростом их концентрации в воде до 100 мг/кг, затем снижаются, при концентрации 500 мг/кг коррозия металла практически прекращается. При давлении 10 МПа скорость коррозии возрастает непрерывно с ростом концентрации нитритов (рис. 1.3). При введении едкого натра пассивирующие свойства нитритов возрастают, а при введении в раствор хлоридов понижаются При добавлении сульфита натрия в раствор, содержащий NaNO2, заметно уменьшается как общая, так и локальная скорость коррозии металла. Наилучший эффект получен при соотношении![]() . (Рис. 1.4)
. (Рис. 1.4)
Возникновению и развитию коррозионного растрескивания углеродистых и слаболегированннх хромистых и хромоникелевых сталей способствует сероводород. Уже при концентрации H2S, равной 0,0002 %, на металлической поверхности возникает межкристаллитная сетка сульфидов. Атомарный водород, образующийся при сероводородной коррозии, может диффундировать в железо, где его часть, находясь в пустотах кристаллической решетки металла может соединяться в молекулы. При скоплении большого количества молекул водорода в пустотах кристаллической решетки на поверхности стали могут образоваться вздутия. Внутри этих вздутий создается давление водорода. Склонность к образованию межкристаллитных трещин в присутствии сероводорода проявляется в слабокислой и щелочной средах.
Большой интерес представляет влияние углекислоты на коррозию металла. Углекислота в растворе диссоциирует не полностью
![]() (1.8)
(1.8)
Наличие буферных свойств раствора затрудняет нейтрализацию угольной кислоты, так как разрядившиеся ионы водорода пополняются новыми за счет дальнейшей диссоциации, и pH среды изменяется незначительно. Атомарный и молекулярный водород восстанавливают и отслаивают оксидные пленки с поверхности металла, вследствие чего кислород через поврежденные участки беспрепятственно поступает к поверхности металла, и коррозия протекает с неизменной скоростью.
С повышением концентрации СO2 в обессоленной воде уже при pH равном 5,7 скорость коррозии стали значительно увеличивается по сравнению со скоростью коррозии при pH = 7. На коррозию заметное влияние оказывает скорость движения потока среды. Так, по данным [7] при движении жидкости скорость общей коррозии углеродистой стали в оборотной воде в 1,4-3,4 раза больше, а в дистиллированной воде в 6-16 раз больше, чем в статических условиях.
В воде, содержащей ионы![]() , отчетливо прослеживается процесс пассивации оборудования. На первом этапе процесс коррозии развивается свободно, а с образованием защитной пленки скорость коррозии резко замедляется . Затем скорость коррозии может несколько повышаться из-за разрушения защитных пленок .
, отчетливо прослеживается процесс пассивации оборудования. На первом этапе процесс коррозии развивается свободно, а с образованием защитной пленки скорость коррозии резко замедляется . Затем скорость коррозии может несколько повышаться из-за разрушения защитных пленок .
В дистиллированной воде скорость коррозии со временем непрерывно растет в связи с отсутствием ионов![]() , образующих защитную пленку на металле, и низким pH дистиллированной воды, равным 5,7-5,9. При таком pH могут образовываться только рыхлые оксидные пленки со слабыми защитными свойствами.
, образующих защитную пленку на металле, и низким pH дистиллированной воды, равным 5,7-5,9. При таком pH могут образовываться только рыхлые оксидные пленки со слабыми защитными свойствами.
Раствор, содержащий NaOH, КОН может вызвать щелочную хрупкость металла как при наличии кислорода, так и при его отсутствии. Опасная концентрация щелочей в растворах для разных марок сталей различна. Так, разрушение стали 18 Cr.SNi происходит уже под действием 1,47 н. гидроксида натрия при температуре 330°С и при отсутствии упаривания. На теплопередающей поверхности за счет упаривания концентрация щелочи может увеличиваться в 50-100 раз.
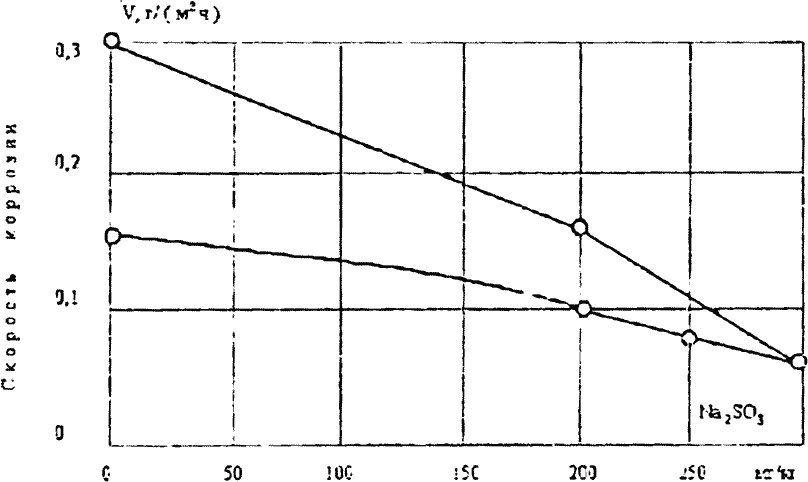
Рис. 1.4. Зависимость скорости нитритной коррозии стали от концентрации сульфита натрия в котловой воде (концентрация в котловой воде нитрита натрия 100 мт/кг). 1,2- при р - 3 и 100 МПа.
Коррозионные процессы идут уже при концентрации свободной щелочи у стенки металла свыше 5% [43]. При концентрации NaOH более 30% и с ростом температуры защитные оксидные пленки растворяются особенно интенсивно с образованием феррита натрия Na2Fe2O4 и гипоферита натрия Na2FeO2. Наличие в обессоленной воде щелочи в малых количествах (менее 100 мг-экв/л) способствует локализация коррозии металла при этом важное значение имеет не абсолютная щелочность воды, а относительная, т.е. доля едкого натра в общем солевом составе котловой воды.

