При простое оборудования коррозия протекает в условиях отвечающих условиям атмосферной коррозии. Такую коррозию можно условно подразделить на три типа [43]:
- “мокрая” коррозия, наблюдается при капельной конденсации влаги. Такие условия могут возникнуть при неполном дренировании воды из поверхностей оборудования или при относительной влажности среды в помещении около 100%;
- “влажная” коррозия, протекающая при относительной влажности в помещении более 40 % под тончайшим слоем электролита, образующегося в результате адсорбционной или химической конденсации;
- “сухая коррозия”.
В энергетической практике эти три типа коррозии не всегда можно разграничить. С изменением влажности в рабочем помещении, при наличии на поверхностях нагрева продуктов коррозии или накипи, способных поглощать влагу, как тип, так и скорость коррозии могут меняться в значительных пределах. Качественная зависимость скорости коррозии от степени увлажнения поверхности металла представлена на рис. 1.5. На участке I еще отсутствует сплошная пленка влаги и коррозию нельзя рассматривать как коррозию в электролите. На участке 2 вследствие адсорбции образуется слой влаги еще невидимый, но уже выполняющий функции электролита и протекает процесс не химической, а электрохимической коррозии. Скорость коррозии резко возрастает. Дальнейшее утолщение слоя влаги (участок 3) снижает скорость коррозии металла из-за затруднения диффузии кислорода через слой влаги большой толщины.
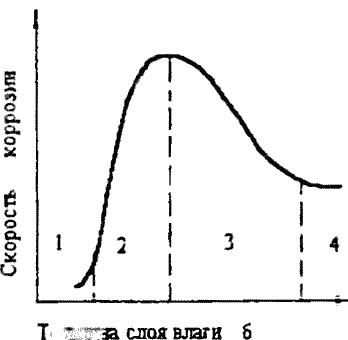
Рис. 1.5. Зависимость скорости атмосферной коррозии от толщины слоя влаги на поверхности металла:
1 - область толщин пленки влаги δ = (1-10)* 10-9м; 2 - δ - 10*10-9 м; 3 - δ = 1мкм - 1мм; 4 - δ > 1 мм.
Наименее опасна коррозия в атмосфере сухого чистого воздуха. На рис. 1.6 приводится зависимость скорости роста защитных оксидных пленок в атмосфере сухого чистого воздуха от продолжительности контакта, разрушение металла идет по чисто химическому механизму взаимодействия кислорода или иных примесей из воздуха с металлом.
Рост пленки осуществляется за счет диффузии электронов атомов или ионов металла через оксидную пленку наружу и с меньшей скоростью за счет диффузии атомов (или ионов) кислорода в обратном направлении. Наиболее вероятно, что зона роста оксидной пленки располагается внутри нее со смещением к внешней поверхности. Интенсивный рост пленки происходит в первые 2-3 ч, после чего ее утолщение практически прекращается. Для нержавеющих сталей толщина пленки в этом случае не превышает (1-2)*109, а для углеродистых - (3-4)*109 м.
Если в воздухе находятся следы сернистых соединений, то размер пленки может увеличиваться до 4*10 8 метра и более за счет того, что сульфид металла имеет значительно большую ионную и электронную проводимость, чем оксид. Однако в сухой атмосфере без влаги этот вид коррозии не опасен и не приводит к заметным коррозионным разрушениям.
Влажная коррозия протекает на поверхности металла с обязательным образованием пленки влаги и при относительной влажности среды более 40%, когда становится возможной конденсация влаги.
Капиллярная конденсация связана с тем, что упругость паров, насыщающих пространство, зависит от кривизны мениска жидкости. Над вогнутым мениском давление насыщенных паров больше, чем над плоским и выпуклым мениском, здесь и происходит преимущественно конденсация влаги. Вогнутый мениск характерен для углубления в металле, щелей, трещин, мест расположения пылинок на металле или пор в оксидной пленке (рис. 1.7).
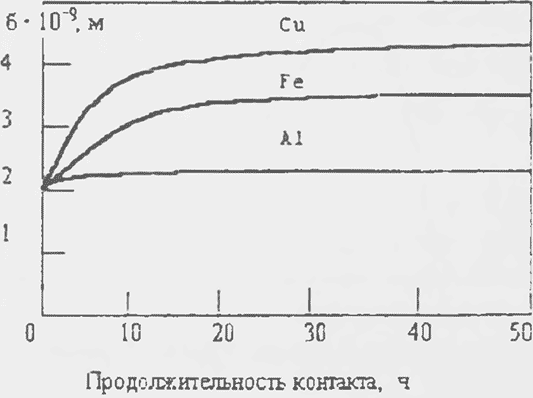
Рис. 1.6 Кинетика роста оксидных пленок на различных металлах при комнатной температуре в кислороде или сухом воздухе (По Кубашевскому и Гопкинсу).

Рис. 1.7. Возможные центры капиллярной конденсации влаги при атмосферной коррозии:
1- щель или зазор в деталях конструкции; 2 - пылинки на поверхности металла; 3 - поры в продуктах коррозии.
Адсорбционная конденсация влаги происходит при условии, если появляются силы сцепления молекул воды с твердой поверхностью (силы адгезии). При относительной влажности менее 100, но более 40%, когда еще отсутствует чисто физическая капельная конденсация, даже на плоской и чистой поверхности адсорбируется слой влаги толщиной в несколько молекулярных слоев. Так, для стали, меди и цинка при относительной влажности воздуха 55 % толщина адсорбционного слоя влаги достигает 15 молекулярных слоев, а при относительной влажности около 100% 20-100 молекулярных слоев [43]. При влажности выше 70% на чистой поверхности металла образуется полимолекулярная пленка воды, благоприятствующая коррозии металла по законам электрохимической кинетики.
При наличии на поверхности металла солевых отложений и продуктов коррозии, способных связываться с водой, происходит химическая конденсация влаги с образованием гидратированных соединений, упругость насыщенных паров над которыми будет гораздо меньше.
В табл 1.1 (приложение) приведены данные об относительной влажности среды, при которой соли начинают растворяться в поглощаемой из воздуха влаге.
Процессы коррозии при влажности более 40% протекают под пленкой влаги в электролите. Критическая влажность может значительно изменяться в зависимости от состояния поверхности металла, наличия отложений солей и продуктов коррозии, способных связываться с водой с образования в среде которого протекает интенсивно развивающаяся коррозия.
В практике, где на стальных поверхностях имеются отложения меди, например в ПВД, деаэраторе.
Авторами исследовалась атмосфера котельного и турбинного цехов на отметках 0 и + 8 на присутствие в воздухе сернистого газа и паров воды (табл. 1.2). Оба показателя непосредственно влияют на процесс коррозии оборудования при его простое. Работа проводилась на трех ТЭС с барабанными котлами при сжигании углей Экибастузского месторождения.
Концентрация сернистого газа в воздухе на отметке 0 выше, чем на отметке + 8. Влажность воздуха в цехе зависит от культуры эксплуатации оборудования, погодных условий и постоянно меняется. При этом в любое время года влажность воздуха в помещения и содержание в нем SO2, SO3 таковы, что имеются условия для протекания интенсивной коррозии оборудования.
Скорость электрохимического процесса, так называемой мокрой коррозии, большинства технически важных металлов, таких, как Fe, Ζη, Си и других, зависит преимущественно от эффективности протекания катодной деполяризации за счет кислорода воздуха. С уменьшением толщины пленки влаги до 30 мкм скорость катодного процесса кислородной деполяризации возрастает из-за малой толщины пленки, препятствующей доступу кислорода воздуха к поверхности катодных участков.
Можно уменьшить влажную и мокрую коррозию металла путем торможения катодного процесса, например, созданием на поверхности металла прочной окисной защитной пленки, уменьшающей доступ кислорода к корродирующей поверхности, или исключением кислорода из окружающей металл среды, например при заполнении объемов оборудования инертным газом - азотом. Эффективным способом снижения такой коррозии следует считать уменьшение электрической проводимости слоя влаги на металле, т е. предварительный вывод солей с поверхности металла перед его остановом.
На катодных участках при деполяризации ионами происходит разряд катионов, например, ионов водорода,
![]() (1.9)
(1.9)
или уменьшение валентности катионов
![]() (1.10)
(1.10)
Кроме того, происходит деполяризация нейтральными молекулами в растворе
![]() (1.11)
(1.11)
Для снижения скорости коррозии на анодных участках необходимо замедлить процесс ионизации металла. Торможение процесса может обеспечиваться малой скоростью диффузии образующихся катионов в толщу раствора. Концентрация ионов металла у поверхности больше, чем в растворе, и возникающая концентрализационная поляризация тормозит диффузию катионов металла в раствор. Кроме того, продукты коррозии металла, образующие защитную пленку, имеют ограниченную растворимость в нейтральных и щелочных средах, что также тормозит анодный процесс.
В кислых средах защитные пленки из оксидов железа имеют малую стойкость, а в щелочных, даже при коррозионно-опасных концентрациях кислорода, коррозионный процесс замедляется, и при pH более 9,8 скорость коррозии стали при всех концентрациях кислорода приближается к нулю.
Часть теплосилового оборудования изготовлена из сплавов на основе меди и также подвергается коррозии в период простоя. При этом медь переходит в раствор с образованием ионов Си2+, удаление которых из пристенного слоя идет за счет перемешивания или присутствия в растворе комплексообразователей. Медь весьма неустойчива в растворах, содержащих аммиак или аммонийные соли, но обладает достаточной стойкостью в разбавленных растворах неокисляющих кислот (HCl, H2SO4, уксусной, лимонной). При контакте с окислителями (Н2O2, O2) скорость коррозии заметно повышается.
В соляной кислоте скорость коррозии меди больше, чем в серной, вследствие образования комплексных соединений (CuCL). В воде, в растворах нейтральных солей и щелочах без доступа окислителей медь устойчива. В растворах комплексообразователей (например, аммиака), особенно при доступе кислорода или наличии окислителей, медь корродирует с образованием комплексных ионов, например![]() .
.
К основным видам аммиачной коррозии латуней относится обесцинкование и коррозионное растрескивание, развивающееся только при наличии внешних или внутренних растягивающих напряжений. Скорость коррозии латуни зависит от концентрации кислорода и аммиака. На рис. 18 представлены кривые зависимости скорости коррозии латуни от содержания аммиака в среде. Угольная кислота в присутствии кислорода вызывает обесцинкование и коррозию латуни. Кислород выступает как деполяризатор катодного участка: на аноде образуются ионы![]() , а на катоде - ионы ОН.
, а на катоде - ионы ОН.
Продуктами коррозии являются сложные гидратно-карбонатные комплексы меди и цинка. Коррозия такого типа интенсивно протекает при конденсации влаги на поверхностях
Состав и минерализованность воды также влияют на скорость коррозии латуни. Так, в слабоминерализованной воде скорость коррозии сплава МН-5-1 не превышает 0,01 мм/год, а при повышении содержания хлоридов до 350-400 мг/кг и более она достигает 0,05 мм/ год; при вялой циркуляции и температурах свыше 50°С развивается язвенная коррозия.
Снижение pH менее 7 и систематические кислотные промывки усиливают обесцинкование латуни.
Скорость коррозии зависит также от соотношения содержания в воде солей временной и постоянной жесткости. При отношении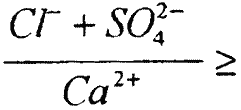 0,1 вода считается коррозионноагрессивной.
0,1 вода считается коррозионноагрессивной.
Наличие в воде бикарбоната кальция способствует образованию на металле защитной пленки СаСO3. Чем выше временная жесткость (щелочность), тем меньшей проницаемостью обладает эта защитная пленка и тем меньше скорость коррозии. Так, при увеличении щелочности воды с 2,5 до 10 мг-экв/кг проницаемость карбонатной защитной пленки снижается в 8 раз.

