ГЛАВА ДЕВЯТАЯ
КОМПОЗИЦИИ МЕТАЛЛ—ОКИСЬ МЕТАЛЛА
9-1. ОБЩИЕ ХАРАКТЕРИСТИКИ
Композиции металл—окись металла отличаются от композиций, рассмотренных в гл. 8, тем, что в качестве тугоплавкой фазы применяется не тугоплавкий металл, а окись металла, способная подвергаться термической диссоциации при температурах контактной дуги. Таким образом, в состав композиции вводится активная составляющая, вызывающая своими продуктами разложения воздействие на контактную дугу.
Установлено, что продукты диссоциации окиси кадмия — пары кадмия и кислород — оказывают гасящее действие на дугу. Аналогичное действие приписывается и другим окислам, выделяющим при разложении только кислород.
Кроме дугогасящего действия, окислы металлов играют роль скелета композиции, хотя они обычно находятся в основном металле в виде отдельно расположенных включений.
В настоящее время известно применение для контактов окислов меди, цинка, кадмия, олова, свинца, висмута, хрома и некоторых других металлов. Наиболее распространены в качестве контактов композиции серебро—окись кадмия.
9-2. КОМПОЗИЦИИ СЕРЕБРО—ОКИСЬ КАДМИЯ
Причиной широкого применения контактов из этой композиции служат особые свойства окиси кадмия (Л. 9-1 и 9-2). Среди окислов металлов окись кадмия отличается сравнительно высокой проводимостью, являясь полупроводником.
В табл. 9-1 даны взятые из разных источников величины проводимости окислов металлов, которые отличаются достаточной тугоплавкостью сравнительно с серебром.
Таблица 9-1
Проводимость и другие свойства окислов металлов

Другим важным свойством, отличающим окись кадмия от окислов других металлов, является диссоциация ее при температуре несколько выше 900°С с образованием одной газообразной фазы, так как точка кипения кадмия лежит при 767° С. Окислы других металлов или не разлагаются при нагревании, или разлагаются па кислород и металл при значительно более высоких температурах. Например, окись цинка возгоняется, не разлагаясь. при 1800° С, окись меди диссоциирует около 1000° С, закиси никеля и железа полностью диссоциируют при нормальном давлении лишь при температурах порядка нескольких тысяч градусов.
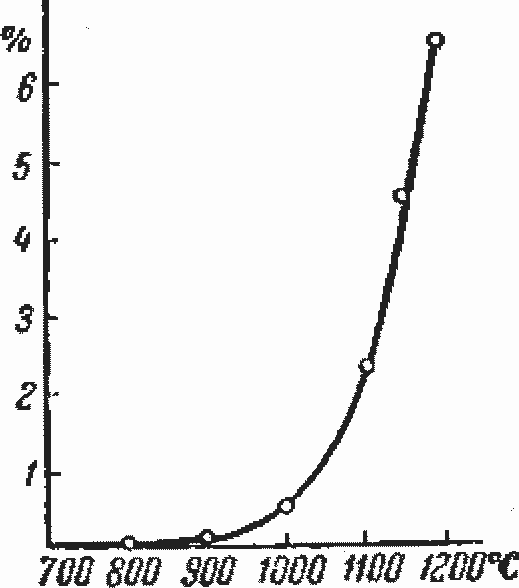
Рис. 9-1. Потери веса окиси кадмия при прокаливании за 30 мин при каждой температуре.
На рис. 9-1 изображена потеря веса порошка окиси кадмия в зависимости от температуры прокаливания. Видно, что энергичное разложение окиси кадмия начинается выше 1000°С. Температура в металлической дуге не ниже 2000° С, поэтому диссоциация зерен окиси кадмия в районе действия дуги должна происходить мгновенно с выделением значительного объема газообразных продуктов. По расчету диссоциации одного зерна окиси кадмия при температурах дуги дает в 104 раз больший объем газообразных продуктов, чем объем окиси. Такое бурное выделение газов механически выдувает дугу, заставляя ее перемешаться по поверхности контакта. В то же время дуга горит в атмосфере паров кадмия и кислорода, потенциал ионизации которых выше, чем паров серебра. Потенциал однократной ионизации атомов серебра 7,54 в, кадмия 8,96 в, а кислорода 13,55 в, вследствие чего дуга в среде продуктов диссоциации окиси кадмия гаснет быстрее, чем в парах серебра. Таким образом, при появлении дуги в момент размыкания контактов зерна окиси, лежащие вблизи ее основания, разлагаются, выдувая и деионизируя дугу и сокращая тем время ее существования.
Микроструктура контакта в районе действия дуги показывает, что вблизи кратера, оставленного дугой, зерна окиси исчезают, но разложение окиси кадмия происходит лишь у самой контактной поверхности. Вследствие мгновенного нагревания дугой лишь самого поверхностного слоя микроструктура основной массы контакта не меняется и тем обеспечивается его термическая устойчивость.
Осадок окиси кадмия, получившийся в результате обратной реакции окисления паров кадмия в области более низкой температуры и осевший на контактах, препятствует их свариванию при замыкании, не нарушая при этом контактной проводимости. Таким образом электропроводность и способность диссоциировать при сравнительно низких температурах (не выше точки плавления серебра) с образованием только газообразных продуктов делают окись кадмия особенно пригодным материалом для контактных композиций рассматриваемого типа.
9-3. МЕТОДЫ ИЗГОТОВЛЕНИЯ КОМПОЗИЦИИ СЕРЕБРО—ОКИСЬ КАДМИЯ
Композиции из серебра с окисью кадмия готовятся двумя принципиально различными способами.
При первом способе в композицию вводится порошок окиси кадмия или металлического кадмия, подвергающегося в дальнейшем окислению в окись, будучи в составе композиции.
Втором способ отличается тем, что кадмии вводится в сплав с серебром и подвергается окислению, будучи в кристаллической решетке сплава. Благодаря атомарному распределению кадмия в решетке при окислении сплава получается значительно более тонкая дисперсность включений окиси кадмия в серебряной матрице.
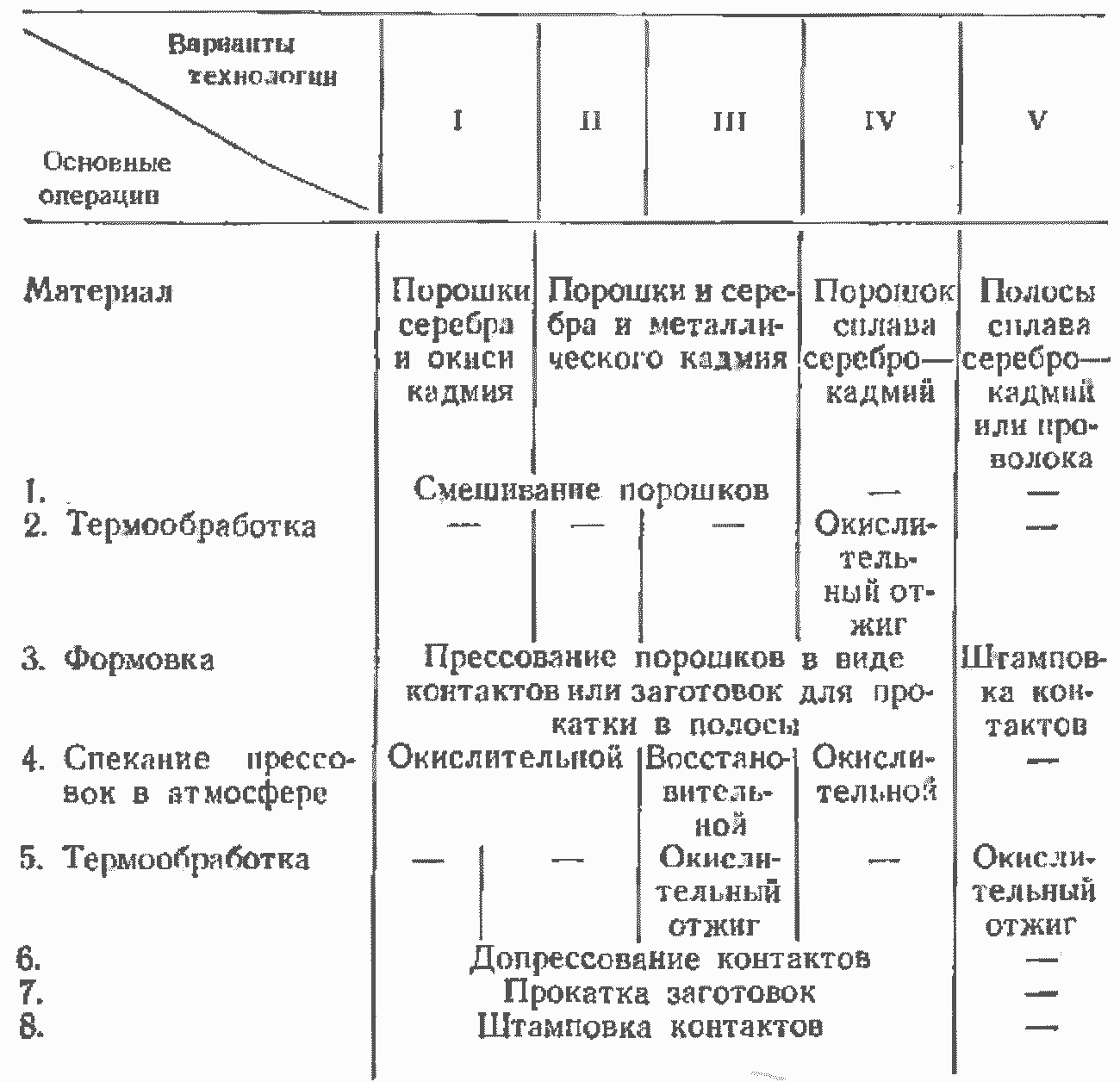
В табл. 9-2 приведены разные варианты технологии получения контактов из композиции серебро — окись кадмия. Принципиально все эти методы применимы для изготовления любых композиций типа серебро — окись металла.
Из табл. 9-2 видно, что пятый метод по технологии значительно проще предыдущих четырех. Вместо порошков применяются полосы или проволока из серебряно-кадмиевого сплава, полученные обычным металлургическим путем. Из полос и проволоки штампуются контакты, которые подвергаются окислительному отжигу [Л. 9-3].
Можно первоначально провести окислительный отжиг полос или проволоки, а затем штамповку контактов.
Таблица 9-2
Схемы технологии изготовления композиций серебро—окись кадмия