Глава III
ХАРАКТЕРИСТИКА РЕАКЦИЙ ПРОЦЕССА ГОРЕНИЯ
1. ГОРЕНИЕ ОКИСИ УГЛЕРОДА
Как показывают многочисленные исследования 124], 125], истинный механизм горения окиси углерода весьма сложен. Макрокинетические характеристики этой реакции, необходимые для приближенного решения поставленной нами задачи, могут быть, однако, получены из работ 151, [19] и [26]. Суммарная скорость реагирования окиси углерода с кислородом, согласно данным этих исследований [19], [26], примерно пропорциональна содержанию окиси углерода при высоких концентрациях кислорода и приближенно — содержанию кислорода при низких (до 4—5%) его концентрациях.
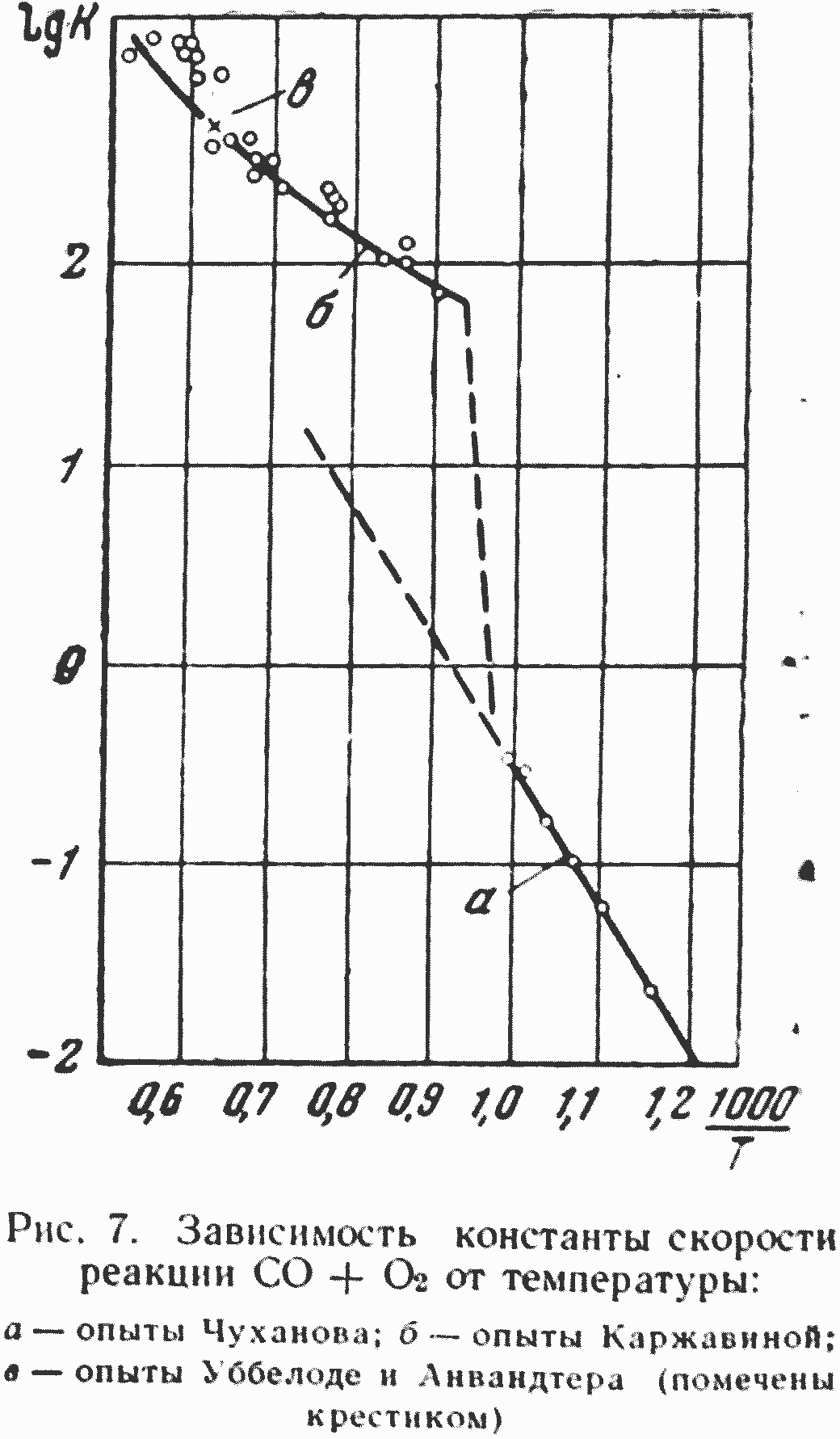
Влияние температуры на удельную константу скорости реакции СО+О3 различно в различных областях температур и, как показывают данные, представленные на рис. 7, можно [21] вывести две различные закономерности, характерные для беспламенного горения, полученного, по экспериментальным данным автора [5], при низких температурах, и высокотемпературного пламенного горения, полученного по данным Каржавиной [19].
Скачок в температурной зависимости, соответствующий примерно 750° (температура воспламенения окиси углерода), разделяет области горения по этим двум законам, отвечающим различным механизмам реакции. Хорошо известно, что при горении газов в узких капиллярах видимое пламя отсутствует; аналогичные условия создаются в зазорах между мелкими твердыми частицами. Беспламенное горение окиси углерода осуществляется также и при низких концентрациях окиси углерода*.
Как показали исследования, температурная зависимость, отвечающая первому закону, может наблюдаться и при высоких температурах, но при беспламенном горении окиси углерода.
Для иллюстрации перехода горения СО из одной области в другую в слое горящего кокса приводим данные опытов Каржавиной [19].
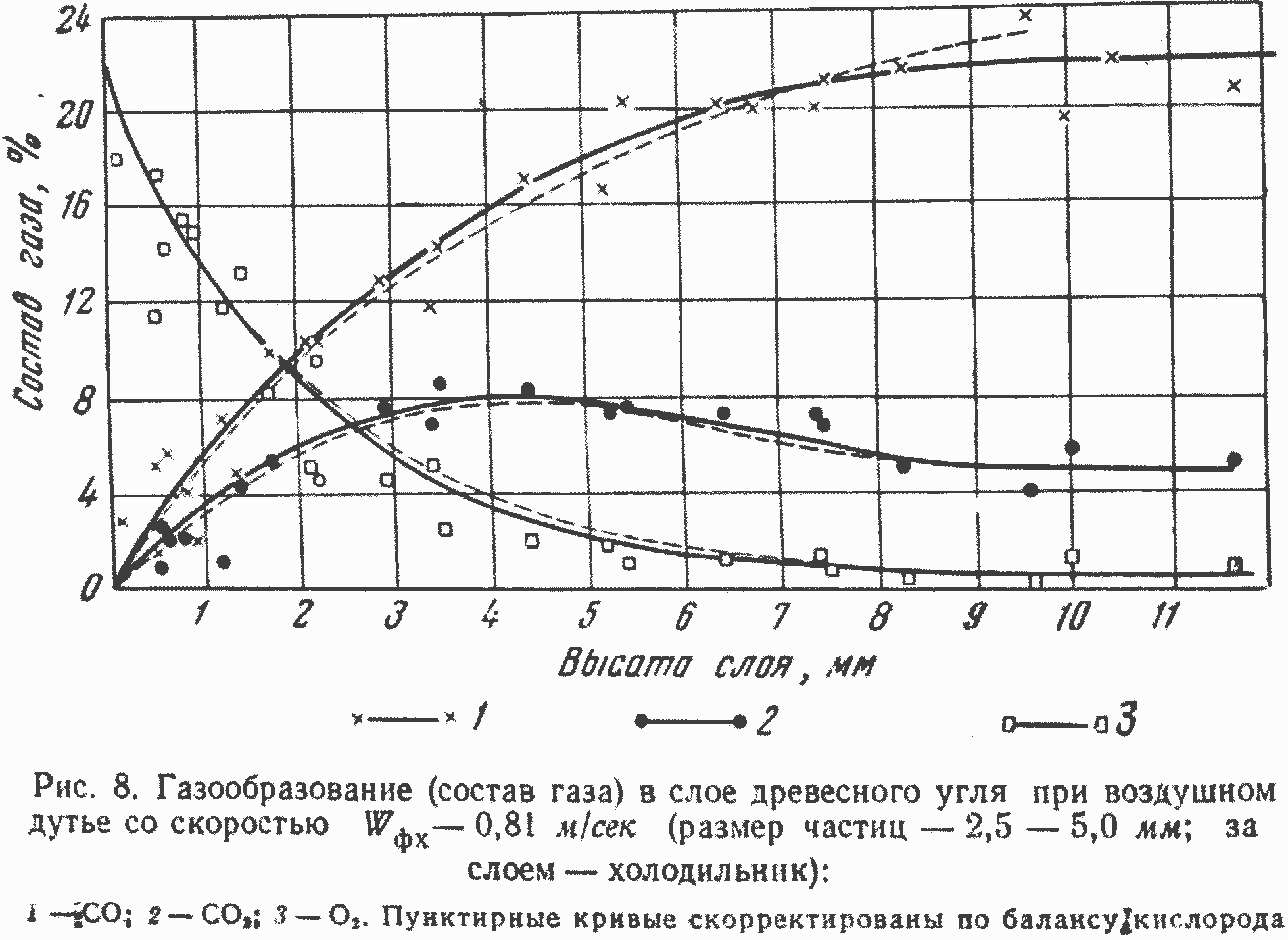
Как известно, при горении слоя мелких частиц (2—4 мм) древесного угля в воздушном дутье (при 1200—1400°С) в кислородной зоне в качестве первичных продуктов образуются и окись и двуокись углерода. При высоких скоростях дутья при скорости холодной фильтрации Wфч около 0,3 м/сек на выходе из кислородной зоны, как показывает рис. 8, отношение СО/CO2 составляет** величину порядка 4—5. В кислородной зоне в газе присутствуют и окись углерода и кислород, но в мелких канальцах между частицами угля пламени не образуется, и окись углерода горит относительно медленно (см. рис. 7).
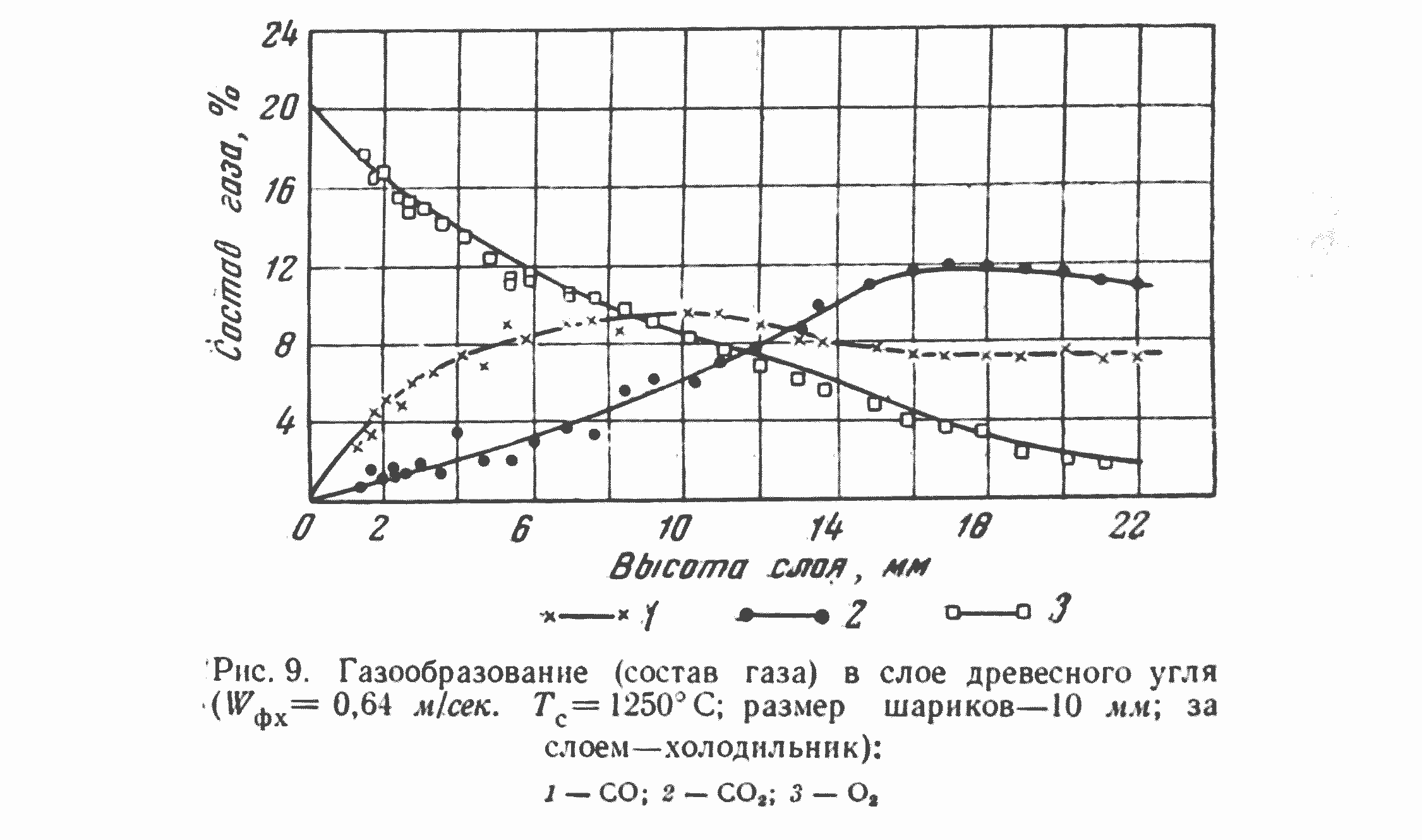
Картина газообразования резко изменяется, когда мы берем более крупные частицы угля. На рис. 9 приведен опыт Каржавиной со слоем сферических 10-мм частичек древесного угля и с высокой скоростью дутья (при 1250 С). Как видно из рисунка, только в начале слоя***, когда концентрация окиси углерода низкая и газовый поток еще холодный (меньше 800°), отношение СО/CO2 относительно высоко (около 3), а затем оно резко падает, и концентрация окиси углерода становится даже ниже, чем двуокиси. В этом случае в более крупных по сечению и объему зазорах между частицами угля наблюдается горение окиси углерода по второму закону (см. рис. 7), протекающее со скоростью большей (на один-два порядка), чем скорость беспламенного горения в зазорах между мелкими частичками угля.
Образование пламени горящей окиси углерода можно наблюдать, если взять горящий слой угольных частиц высотой меньше кислородной зоны. В этом случае при высокой скорости дутья на выходе из слоя хорошо видны языки пламени горящей окиси углерода, и если взять за пламенем пробу газа, то в ней обнаруживаются практически только CO2 и О2, в то время как проба, отобранная непосредственно за слоем углерода в тонкую охлаждаемую трубку, показывает наряду с присутствием кислорода значительную концентрацию окиси углерода.
Таким образом, сохранение (вынос из кислородной зоны) первичной окиси углерода, т. е. организация и осуществление процесса так называемой высокоскоростной газификации (по З. Ф. Чуханову), возможно только в плотном слое мелких частиц или вообще в слое топлива (кокса), где образуются мелкие зазоры (межкусковые объемы), т. е. содержащие наряду с более крупными частицами также мелкие, частично заполняющие пустоты между более крупными кусками.
В слое крупных фракционированных частиц (кусков) кокса (угля) вынос окиси углерода осуществить значительно труднее, так как в этом случае она горит с очень высокой скоростью. Как же будет обстоять дело в случае важном для подземной газификации, например при работе по методу потока, когда горение кокса идет в канале, имеющем размеры больше, чем 10 и даже 50— 100 мм?
Если взять короткий канал (трубку) из электродного угля диаметром 2—4 мм и продувать его с большой скоростью горячим воздухом, то на выходе будет наблюдаться характерный факел горящей окиси углерода;
однако если диаметр углеродного канала увеличить до 20—25 мм и даже до 10—12 мм, такой факел пропадает, и пламя может наблюдаться только вблизи поверхности углерода. Пламя горящей окиси углерода на выходе из кислородной зоны канала исчезает и при малых скоростях дутья.
В широком углеродном канале (свыше 7—15 мм) и при малых скоростях дутья (ламинарный режим) первичная окись углерода сгорает вблизи поверхности углерода, и создается внешнее впечатление, что первичным продуктом горения углерода при этом является только двуокись углерода.
На рис. 10 представлены результаты работы Цухановой [21] по изучению газообразования при ламинарном горении углеродного канала и изменении температуры горящей поверхности углерода. Как видно из рисунка кислород при горении углеродной стенки канала практически полностью расходуется на образование двуокиси углерода, так как концентрация окиси углерода в газе не превышает 2% даже при температуре 1400 , когда концентрация кислорода в газе ниже 2%.
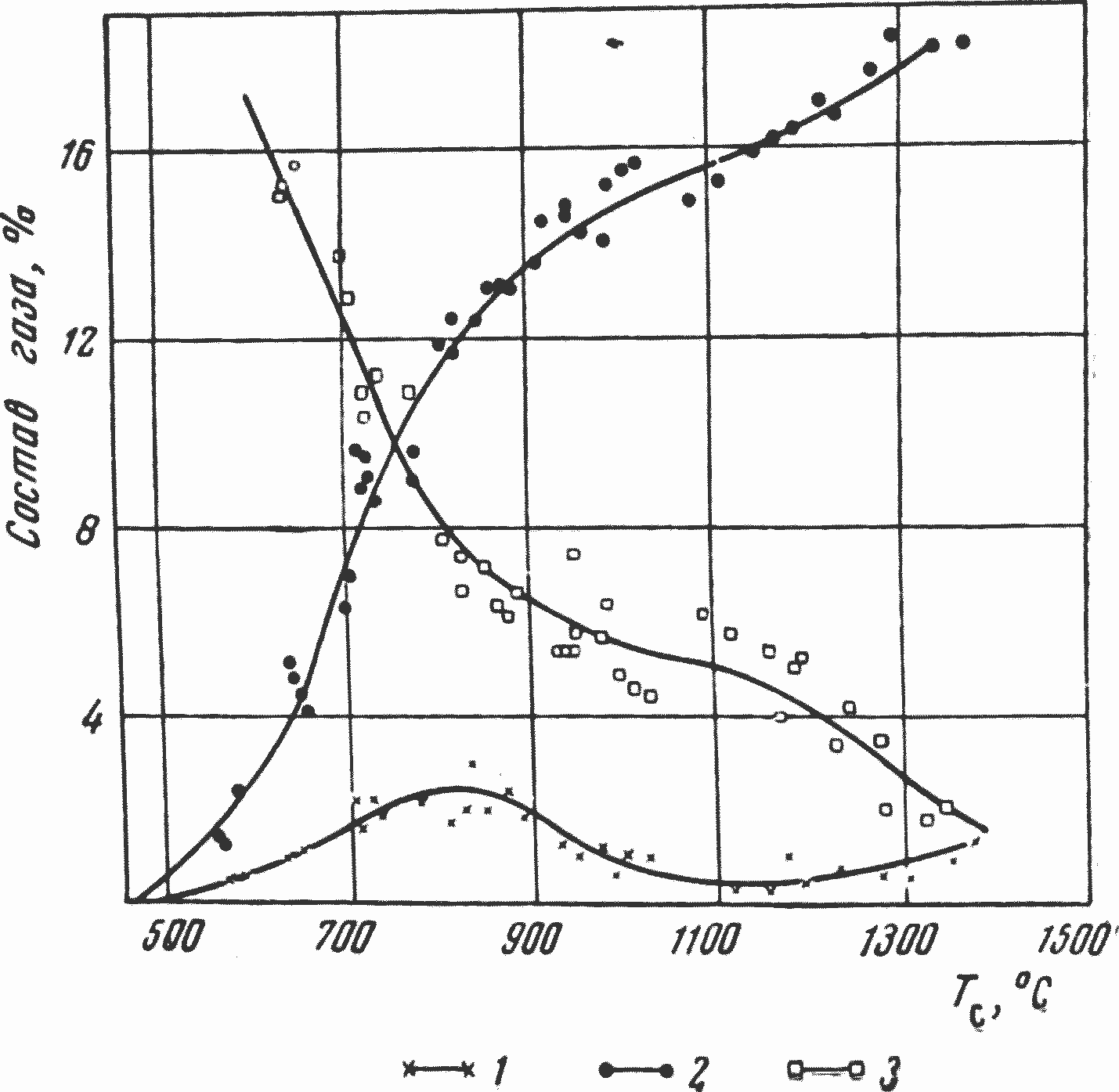
Рис. 10. Влияние температуры поверхности горящего канала на газообразование (состав газа) при ламинарном режиме (d канала = 12 мм; длина канала — 950 мм; расход воздуха 20 л/мин):
1 — СО; 2 — CO2; 3 — О2
К сожалению, точных экспериментальных исследовании горения углеродного канала больших размеров (20 500 мм) нет, что является крупным упущением в работах исследовательских организаций по п. г. у. Единственной сколько-нибудь надежной работой по изучению процесса горения углеродного канала при турбулентном режиме, кроме сравнительно кратких исследований Цухановой, является работа Гольденберга [28], который провел исследование горения стенок канала электродного угля (d=16 мм) при изменении критерия Re от 4000 до 25 000. Подробные исследования концентрационных полей убедительно показали, что при всех исследованных режимах образующаяся при первичном реагировании углерода окись углерода успевает сгореть в кислородной зоне на сравнительно небольшом расстоянии от поверхности.
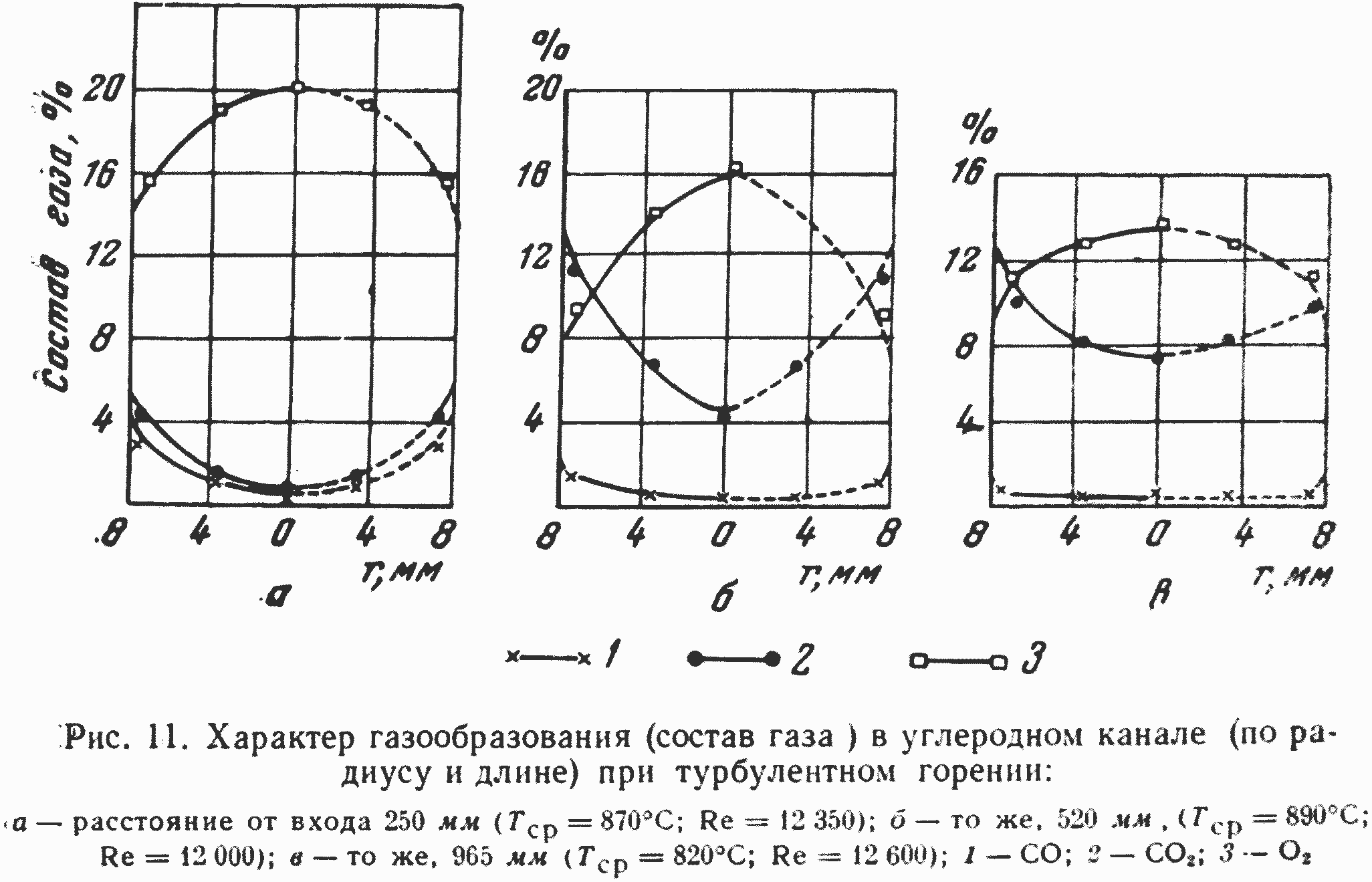
На рис. 11 показан характер газообразования в горящем углеродном канале диаметром 16 мм при температуре 900° и при значении Re 12 000. Как видно из рисунка, даже при высокой скорости дутья (70 м/сек) и сравнительно низкой температуре окись углерода практически полностью сгорает на небольшом расстоянии от углеродной поверхности. Только в начале канала, когда дутье еще имеет относительно невысокую температуру и концентрация СО низка, часть окиси углерода сохраняется не сгоревшей.
Можно с достаточной уверенностью утверждать, что при больших размерах каналов практически во всем газовом объеме кислородной зоны канала окись углерода будет отсутствовать в сколько-нибудь заметных концентрациях и единственным (хотя и не первичным) обнаруживаемым в газовом объеме продуктом горения будет двуокись углерода.
Таким образом, можно сделать вывод, что в горящем углеродном канале (достаточно большого диаметра), т. е. в кислородной зоне подземного газогенератора, работающего по методу потока или скважин, вторичная реакция горения окиси углерода практически всегда протекает до конца и тем самым играет пассивную роль, не влияя на характер изменения состава газа, .получаемого в подземном газогенераторе.
Кинетические характеристики реакции горения окиси углерода не имеют какого-либо значения для расчета процесса подземной газификации в углеводном канале, так как эта реакция при всех практически существующих условиях успевает завершиться в небольшой пристеночной части объема кислородной зоны. Этот вывод имеет большое практическое значение, поскольку расчеты интенсивности горения углеродного канала в этих условиях значительно упрощаются, и можно без особой ошибки принимать, что на поверхности канала образуется только двуокись углерода.
Для того, чтобы решить вопрос о значении реакции горения окиси углерода для других методов подземной газификации угля и, в частности, метода фильтрации, необходимо более детально рассмотреть как все первичные и вторичные реакции горения углерода, так и конкретные условия организации этого метода.
В заключение кратко коснемся вопроса о возможности образования при методе потока (газификации в канале) переходной кислородной зоны, смешанной с зоной восстановления. Такую возможность часто предполагают исследователи п. г. у., обосновывающие ее следующими рассуждениями. В углеродном канале, имеющем, например, одну углеродную стенку, кислород воздуха, протекающего по каналу, реагирует с углеродом на определенной протяженности канала, а затем схема процесса горения постепенно изменяется, и горение идет так, как это было показано на рис. 6 (горение частицы углерода осуществлялось за счет реагирования и с О2 и с CO2). При этом кислород в газовом объеме реагирует главным образом с окисью углерода.
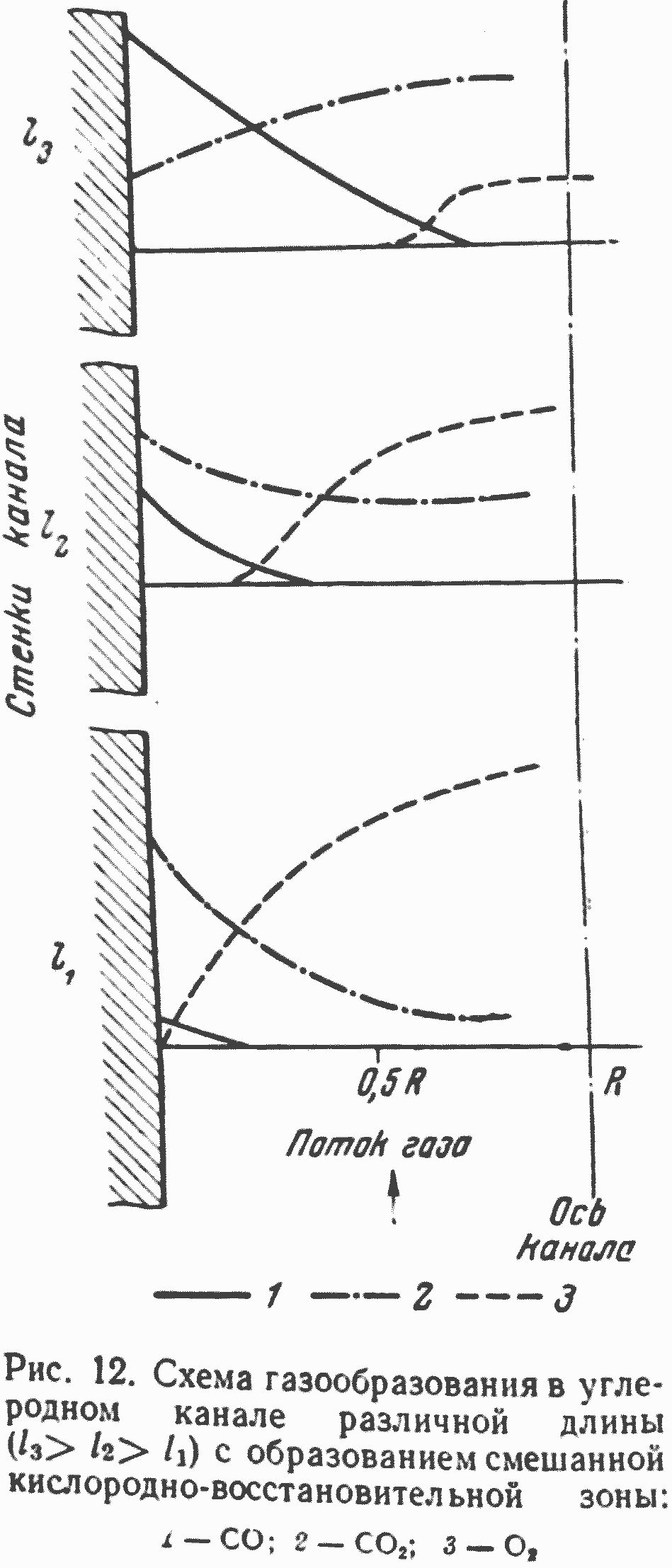
Схема газообразования при таком процессе в канале представлена на рис. 12. По этой схеме наряду с кислородной зоной появляется кислородновосстановительная смешанная зона, отличающаяся тем, что на поверхности кокса в ней идет не взаимодействие углерода с кислородом, а восстановление CO2 углеродом. Таким образом, часть сечения канала занимает горючий газ, а другую часть, удаленную от углеродной стенки, занимает газ с высокой концентрацией кислорода.
Для того чтобы определить условия, при которых осуществим такой процесс горения по схеме Бурке и Шумана 123], необходимо произвести расчет, аналогичный тому, который представлен на рис. 6.
Однако даже без расчета по аналогии: с горением частицы (рис. 6), можно сказать, что такое горение стенки канала подземного газогенератора с практически заметным эффектом возможно только при весьма высоких температурах, близких к 1700—2000 °C, да и тогда, очевидно, только часть углерода, в связи с спецификой температурного режима,, будет расходоваться по реакции восстановления двуокиси углерода, т. е. по редукционной схеме Бурке и Шумана, а другая часть на всем протяжении кислородной зоны будет выгорать за счет реагирования со свободным кислородом.
Для расчета процесса горения в кислородной зоне с участием реакции. CO2 + С и процесса газификации кокса в восстановительной зоне за счет реакции CO2 + С, являющейся, конечно, важнейшей реакцией газогенераторного- процесса, необходимо достаточно подробно рассмотреть механизм и кинетику этой, на первый взгляд достаточно простой, в действительности же весьма сложной гетерогенной реакции.

